
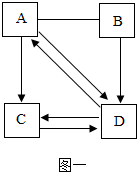
 某化学兴趣小组的同学在老师的指导下,开展如下探究活动.
某化学兴趣小组的同学在老师的指导下,开展如下探究活动. | OH- | NO3- | Cl- | SO42- | CO32- |
| H+ | 溶、挥 | 溶、挥 | 溶 | 溶、挥 | |
| Na+ | 溶 | 溶 | 溶 | 溶 | 溶 |
| Ca2+ | 微 | 溶 | 溶 | 微 | 不 |
| Ba2+ | 溶 | 溶 | 溶 | 不 | 不 |
| Mg2+ | 不 | 溶 | 溶 | 溶 | 微 |



科目:初中化学 来源: 题型:
| A、为了节约粮食,受到黄曲霉毒素污染的大米可以食用 |
| B、青少年正处于生长发育期,应多食用含有蛋白质的食物,越多越好 |
| C、人体缺乏维生素C,会引起坏血病,因此应经常食用新鲜水果和蔬菜 |
| D、鸦片、吗啡等具有镇静、止痛和兴奋作用,学习累了可以喝点提神 |
查看答案和解析>>
科目:初中化学 来源: 题型:
 如图 是甲、乙两种固体物质的溶解度曲线,回答:
如图 是甲、乙两种固体物质的溶解度曲线,回答:查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验操作 | 实验现象 | 实验结论 |
| 取少量白色固体放入试管中,滴加稀盐酸. | 猜想二不成立:不是CaCO3. | |
| 取少量白色固体加入到水中,取上层清液, | 猜想三成立:白色固体是Ca(OH)2 |
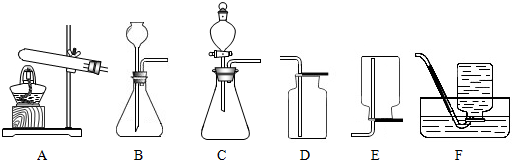
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
 2014年3月22日是第二十二届“世界水日”,水与人类的生活和生产密切相关,请回答下列问题:
2014年3月22日是第二十二届“世界水日”,水与人类的生活和生产密切相关,请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
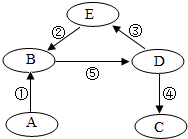 已知A、B、C、D、E五种物质都有人体内含量最高的一种金属元素,其中A是单质,B、C含有两种元素,D、E含有三种元素,反应⑤是放热反应,它们之间的转化关系如图所示,下列推理不正确的是( )
已知A、B、C、D、E五种物质都有人体内含量最高的一种金属元素,其中A是单质,B、C含有两种元素,D、E含有三种元素,反应⑤是放热反应,它们之间的转化关系如图所示,下列推理不正确的是( )| A、E是碳酸钙 |
| B、反应④一定是中和反应 |
| C、反应③可以由多个化学反应实现 |
| D、反应②是吸热反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com