
分析 在实验室制取气体,“制取”包括发生装置和收集装置,根据确定发生装置与收集装置的思路,进行分析解答.
解答 解:因为发生装置的选定与反应物的状态和反应条件有关.如反应物是固体+液体反应,不需加热,属于固液常温型制取气体;反应物都是固体,且需要加热,属于固体加热型,需要选用有酒精灯等加热装置的装置.故确定某种气体的发生装置时,需要考虑的因素是反应物的状态和反应条件.
实验室制取气体收集方法的选择是根据:一般考虑气体物理性质中的密度和溶解性;难溶于水或不易溶于水且不与水反应的气体可用排水法收集;密度比空气大的气体(不能与空气中的成分反应)可用向上排空气法收集,密度比空气小的气体(不能与空气中的成分反应)可用向下排空气法收集.
故答案为:反应物的状态;反应条件;密度;溶解性.
点评 本题难度不大,掌握实验室制取气体的一般思路(制取装置与收集装置的确定方法)是正确解答本题的关键.


科目:初中化学 来源: 题型:选择题
| A. | ①③ | B. | ②③ | C. | ①④ | D. | ②④ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | H2SO4 | B. | Na2SO4 | C. | HCl | D. | CuCl2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
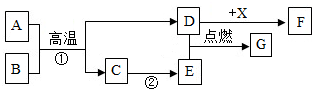
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
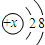 ,若X等于11,则该微粒表示阳(填“阳”或“阴”)离子.
,若X等于11,则该微粒表示阳(填“阳”或“阴”)离子.查看答案和解析>>
科目:初中化学 来源: 题型:多选题
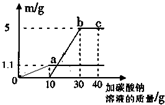 小红取实验室制CO2反应后的废液25g,逐滴加入质量分数为26.5%的碳酸钠溶液.他根据实验测得的数据绘出如图,其中纵坐标m是实验得到的沉淀或气体的质量,横坐标表示的是碳酸钠溶液质量.下列说法正确的是( )
小红取实验室制CO2反应后的废液25g,逐滴加入质量分数为26.5%的碳酸钠溶液.他根据实验测得的数据绘出如图,其中纵坐标m是实验得到的沉淀或气体的质量,横坐标表示的是碳酸钠溶液质量.下列说法正确的是( )| A. | 图中oa段表示反应生成沉淀 | B. | c点表示溶液PH>7 | ||
| C. | 废液中HCl质量分数为7.3% | D. | a点溶液中的溶质有3种 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
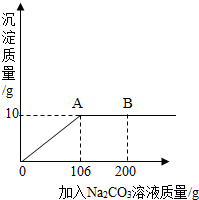 氯化钙钾石的化学式为KCl•xCaC12(x是CaCl2的系数).它是一种天然的钾肥,溶于水后得到KCl与CaCl2的混合溶液.某化学兴趣小组为了测定氯化钙钾石中钾元素的质量分数,称取样品18.55g加水完全溶解得到KCl与CaCl2的混合溶液,向该溶液中逐滴加入Na2CO3溶液,产生的沉淀与加入Na2CO3溶液的质量关系如图所示.请回答下列问题:
氯化钙钾石的化学式为KCl•xCaC12(x是CaCl2的系数).它是一种天然的钾肥,溶于水后得到KCl与CaCl2的混合溶液.某化学兴趣小组为了测定氯化钙钾石中钾元素的质量分数,称取样品18.55g加水完全溶解得到KCl与CaCl2的混合溶液,向该溶液中逐滴加入Na2CO3溶液,产生的沉淀与加入Na2CO3溶液的质量关系如图所示.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com