
【题目】(6分)请用化学方程式解释下列问题:
(1)稀硫酸可用来除铁锈:__________
(2)氢氧化钠溶液敞口放置变质:________
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:初中化学 来源: 题型:
【题目】有①镊子、②烧杯、③试管、④胶头滴管、⑤药匙、⑥燃烧匙、⑦坩埚钳、⑧10mL量筒、⑨100mL量筒、⑩托盘天平等仪器.
请为下列实验操作选仪器(填写相应的序号):吸取或滴加少量液体时用 ;可以直接在酒精灯火焰上加热的玻璃仪器是 ;夹持镁带燃烧用 ;取用石灰石块可用 ;量取8mL的水用 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(8分)提纯含少量泥沙的粗盐,一般经过以下操作流程:
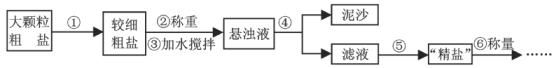
(1)操作①中必须用到的一种仪器是 (填序号)。
A.研钵 B.量筒 C.烧杯 D.试管
(2)完成该实验部分操作过程如图所示,其有明显错误的是 (填字母序号)。
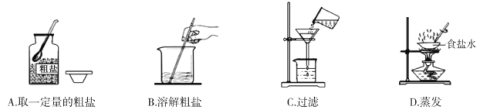
(3)为尽量减少蒸发时发生飞溅,操作⑤中除连续搅拌外还可采取 等措施。
(4)用提纯得到的“精盐”配制了50 g 5%的氯化钠溶液。经检测,溶质质量分数偏小,其原因可能有 (填序号)。
①氯化钠固体仍然不纯
②称量时砝码端忘垫质量相同的纸片
③量取水时,仰视读数
④装瓶时,有少量溶液洒出
(5)粗盐中除含泥沙等不溶性杂质外,还含有少量的MgCl2、CaCl2等可溶性杂质;为了得到较纯净的氯化钠,除去泥沙的“精盐”又作了如下处理(假定杂质只有MgCl2、CaCl2两种;反应中所加试剂均过量)。
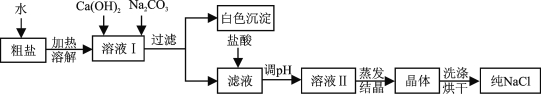
①白色沉淀含有物质的化学式为 ;
②在得到的滤液中加入过量盐酸的目的是 ;
③选用蒸发结晶法而不用降温结晶法的理由是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学就在我们身边,它与我们的生活息息相关.
(1)由生铁制成的铁制品极易生锈,生铁属于 (填“合金”或“纯金属”),生铁生锈的条件是 .
(2)炒菜时铁锅中的油着火可用锅盖盖灭.其原理是 .
(3)市场上流行的一种口罩中使用了活性炭,这是利用了活性炭的 作用.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(13分)某品牌纯碱中含有少量氯化钠.某化学探究小组欲测定该品牌纯碱的纯度(即碳酸钠的质量分数)。
Ⅰ.甲组同学设计如图所示实验:

【实验步骤】①组装好如图仪器,并 ;
②称取7.0g样品放入锥形瓶中,加入少量蒸馏水溶解,并在其他装置中加入相应的药品;
③称量装置C的质量;
④打开分液漏斗旋塞滴入稀硫酸,直到不再产生气泡为止;
⑤再次称量装置C 的总质量; ⑥计算出样品中碳酸钠的质量分数。
【实验分析】(1)A装置中反应的化学方程式为 ;
(2)B装置的作用是 ;
(3)如果没有D装置则所测样品中碳酸钠的质量分数偏大的原因是 ;
(4)称得纯碱样品的质量为7.0g,实验前、后C装置(包含药品)的质量分别为61.2g和63.4g,则该纯碱样品的纯度为 (计算结果精确到0.1%)。
Ⅱ.乙组同学采用生成沉淀的方法来测定样品中纯碱的质量分数,设计了如下实验:
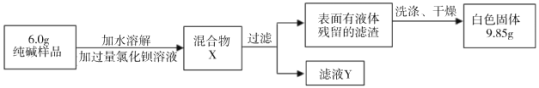
(1)判断加入氯化钡溶液是否过量的合适方法是 (填编号),然后观察现象判断。
A.向混合物X中滴加稀硫酸,若有白色沉淀生成则说明氯化钡已经过量
B.静置混合物X,向上层清液中继续滴加氯化钡溶液,若无白色沉淀生成,则氯化钡已经过量
(2)判断滤渣是否洗涤干净,可以采取向最后的洗出液中滴加 ,然后观察现象判断。
(3)根据实验数据,乙组测得样品中碳酸钠的质量分数为多少?(写出计算过程,计算结果精确到0.1%)。
【实验反思】乙组所测实验数据比甲组更准确,你认为甲组存在较大偏差的原因可能是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(5分)海洋是人类宝贵的自然资源,从海水中可以得到粗盐。
(1)称取5.0g粗盐,逐渐加入10mL水中,边加边用玻璃棒搅拌,一直加到粗盐不再溶解为止。还需要进行的实验步骤依次为:①称量剩余粗盐、② 、③ 、④称量精盐、⑤计算产率。
(2)下图是某工厂利用粗盐水生产纯碱的工艺流程图。
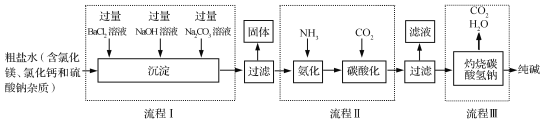
①下列说法正确的是 (填字母)。
A.流程Ⅰ中加入溶液的顺序不能改变
B.流程Ⅰ将粗盐水中的SO42-、 Mg2+、Ca2+转化为沉淀
C.流程Ⅰ后过滤得到三种沉淀
D.流程Ⅲ中发生的是分解反应
②流程II中发生的主要反应为NH3+CO2+H2O NH4HCO3 ,
NH4HCO3+NaCl NaHCO3↓+NH4Cl 。
20℃时,向100g水中加入11.7g NaCl和15.8g NH4HCO3,充分反应后,理论上从溶液中析出晶体的质量为 g(20℃时,NaHCO3的溶解度为9.7g, NH4Cl的溶解度为37.2g)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2015年1月起,国内重型柴油机普推国IV排放标准。减排的原理为:向反应罐内喷入车用尿素溶液,在一定条件下,尿素【CO(NH2)2】先转化为NH3,NH3再与发动机排出的NO等反应生成氮气和水。回答下列问题:

(1)尿素属于 (填“有机物”或“无机物”)。
(2)尿素的下列性质中,属于化学性质的是 (填字母)。
A.无色晶体 B.熔点132.7℃
C.易溶于水 D.加热超过熔点即分解
(3)以尿素为主要原料制成的某些塑料是热固性塑料,该塑料 (填“能”或“不能”)用加热法修补。
(4)NH3与NO在一定条件下反应的化学方程式为 。
(5)过期的车用尿素溶液可用作氮肥。根据右图标签,该桶溶液(假设尿素没有损耗)能供给作物约 Kg(填字母)氮元素。
A.1.5 B.3.0 C.6.5
(6)喷入反应罐内的尿素溶液不能过多或过少。如果喷入过多,会造成 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com