

·ÖĪö µēŹÆ¶Ō“ó¼Ņ±Č½ĻÄ°Éś£¬µ«ŹĒĢāÄæøų³öĮĖ»ÆѧŹ½£®ÓÉÓŚŗĶŃõĘų³ä·ÖČ¼ÉÕ£¬ĖłŅŌÉś³ÉµÄĪŽÉ«ĘųĢåÓ¦øĆŹĒ¶žŃõ»ÆĢ¼£¬Ķ¬Ź±øĘŌŖĖŲŗĶŃõŌŖĖŲŠĪ³ÉµÄ°×É«¹ĢĢåĪļÖŹÓ¦øĆĪŖŃõ»ÆøĘ£¬¶ųŃõ»ÆøĘĒ”ŗĆÄÜŗĶĖ®·“Ó¦£®µēŹÆŗĶĖ®µÄ·“Ó¦£¬ĢāÄæøų³öµÄŠÅĻ¢ŹĒĻąµ±µēĄėµÄĒāĄė×ÓŗĶĒāŃõøłĄė×Ó·¢ÉśµÄĄė×Ó½»»»£¬ĖłŅŌÓ¦øĆŹĒĢ¼ŌŖĖŲŗĶĒāŌŖĖŲ½įŗĻ£¬¶ųøĘŌŖĖŲŗĶĒāŃõøł½įŗĻ£¬ĖłŅŌÉś³ÉĪļĪŖĒāŃõ»ÆøĘ£ØŅ²ŃéÖ¤ĮĖwæÉŅŌĪŖŃõ»ÆøĘ£©ŗĶC2H2£®C2H2ŗĶŃõĘųÄÜ·“Ӧɜ³É¶žŃõ»ÆĢ¼ŗĶĖ®£®
½ā“š ½ā£ŗĢ¼»ÆøĘ£¬Ė×ĆūµēŹÆ£¬³É·ÖĪŖCaC2£®ÓÉÓŚŗĶŃõĘų³ä·ÖČ¼ÉÕ£¬ĖłŅŌÉś³ÉµÄĪŽÉ«ĘųĢåÓ¦øĆŹĒ¶žŃõ»ÆĢ¼£¬Ķ¬Ź±øĘŌŖĖŲŗĶŃõŌŖĖŲŠĪ³ÉµÄ°×É«¹ĢĢåĪļÖŹÓ¦øĆĪŖŃõ»ÆøĘ£¬¶ųŃõ»ÆøĘĒ”ŗĆÄÜŗĶĖ®·“Ó¦£®µēŹÆŗĶĖ®µÄ·“Ó¦£¬ĢāÄæøų³öµÄŠÅĻ¢ŹĒĻąµ±µēĄėµÄĒāĄė×ÓŗĶĒāŃõøłĄė×Ó·¢ÉśµÄĄė×Ó½»»»£¬ĖłŅŌÓ¦øĆŹĒĢ¼ŌŖĖŲŗĶĒāŌŖĖŲ½įŗĻ£¬¶ųøĘŌŖĖŲŗĶĒāŃõøł½įŗĻ£¬ĖłŅŌÉś³ÉĪļĪŖĒāŃõ»ÆøĘ£ØŹĒČżÖÖŌŖĖŲ×é³É£¬Ņ²ŃéÖ¤ĮĖwæÉŅŌĪŖŃõ»ÆøĘ£©ŗĶC2H2£®C2H2ŗĶŃõĘųÄÜ·“Ӧɜ³É¶žŃõ»ÆĢ¼ŗĶĖ®£®
£Ø1£©Š“¶ŌÓ¦ĪļÖŹµÄ»ÆѧŹ½ĪŖ£ŗW CaO£» X CO2£» Y Ca£ØOH£©2£»Z C2H2£®
£Ø2£©¹żĮ涞Ńõ»ÆĢ¼ĶØČėµ½³ĪĒåŹÆ»ŅĖ®£¬ĻČ»ė×Ēŗó³ĪĒ壬ŹĒŅņĪŖ×īÖÕÉś³ÉĮĖæÉČÜŠŌµÄĢ¼ĖįĒāøĘ£®Ęä·½³ĢŹ½ĪŖ£ŗ2CO2+Ca£ØOH£©2=Ca£ØHCO3£©2£®£ØÉóĢāŹ±×¢Ņā”°¹żĮæ”±Ņ»“ŹµÄ“ęŌŚ£©
¹Ź“š°øĪŖ£ŗ
£Ø1£©CaO£»CO2 £»Ca£ØOH£©2£»C2H2£®
£Ø2£©CO2+Ca£ØOH£©2=CaCO3”ż+H2O£»CaCO3+H2O+CO2=Ca£ØHCO3£©2£®
µćĘĄ ¶ŌÓŚ³öĻÖÄ°ÉśĪļÖŹµÄĶʶĻĢā£¬Ņ»°ćæ¼²éÄŚČŻÓ¦øĆŹĒ½ĻĪŖŹģĻ¤µÄ£¬ĖłŅŌ²»ŅŖĪ·¾å£¬ĀżĀżŹįĄķ£¬Ö®ŗó“ųČė¶ŌÕÕ¼“æÉ£®


 Źī¼ŁĻĪ½ÓÅąÓŽĢ²ÄÕć½¹¤ÉĢ“óѧ³ö°ęÉēĻµĮŠ“š°ø
Źī¼ŁĻĪ½ÓÅąÓŽĢ²ÄÕć½¹¤ÉĢ“óѧ³ö°ęÉēĻµĮŠ“š°ø ŠĄÓļĪÄ»ÆæģĄÖŹī¼ŁÉņŃō³ö°ęÉēĻµĮŠ“š°ø
ŠĄÓļĪÄ»ÆæģĄÖŹī¼ŁÉņŃō³ö°ęÉēĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ėü²»ÄÜÓėŹÆ»ŅĖ®·“Ó¦ | |
| B£® | ³¬ĮŁ½ē¶žŃõ»ÆĢ¼ŹĒŗĻ³ÉµÄŅ»ÖÖŠĀĪļÖŹ | |
| C£® | ³¬ĮŁ½ēCO2Į÷ĢåŠŌÖŹĢŲŹā£¬µ«ĖüÓėøɱłµÄ»Æѧ×é³ÉĻąĶ¬ | |
| D£® | ³¬ĮŁ½ēCO2Į÷ĢåŹĒŅ»ÖÖĢŲŹāµÄĪļÖŹ£¬ČŻŅ×Č¼ÉÕ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĢśĖæŌŚŃõĘųÖŠČ¼ÉÕ£ŗŅų°×É«¹ĢĢå¾ēĮŅČ¼ÉÕ£¬»šŠĒĖÄÉ䣬·Å³ö“óĮæµÄČČ£¬Éś³ÉŗŚÉ«¹ĢĢå | |
| B£® | øßĪĀĢõ¼žĻĀľĢ滹ŌŃõ»ÆĶ£ŗŗŚÉ«¹ĢĢåÖš½„±ä³É¹āĮĮµÄĶ | |
| C£® | µē½āĖ®ŹµŃé£ŗĮ½øöµē¼«ø½½ü²śÉśĘųÅŻ£¬Ņ»¶ĪŹ±¼äŗó£¬Õż”¢øŗ¼«²śÉśµÄĘųĢåĢå»ż±ČŌ¼ĪŖ2£ŗ1 | |
| D£® | Ķʬ·ÅČĖĻõĖįŅųČÜŅŗÖŠ£ŗ×ĻŗģÉ«¹ĢĢå±ķĆęÓŠŅų°×É«¹ĢĢå²śÉś£¬ČÜŅŗÓÉĄ¶É«Öš½„±äĪŖĪŽÉ« |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | æÉÄÜ“ęŌŚCl- | B£® | Ņ»¶Ø“ęŌŚCO32-£¬Ņ»¶Ø²»“ęŌŚBa2+ | ||
| C£® | Ņ»¶Ø“ęŌŚNa+ | D£® | Ņ»¶Ø“ęŌŚSO42-£¬æÉÄÜ“ęŌŚCa2+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢ½¾æĢā
| ŹµŃé»ģŗĻČÜŅŗ | 1 | 2 | 3 | 4 | 5 | 6 |
| ±„ŗĶĮņĖįĶČÜŅŗ/mL | 0 | 0.5 | 2.5 | 5 | 10 | 20 |
| Ė®/mL | 20 | 19.5 | 17.5 | V | 10 | 0 |
| ŹµŃé1 | ŹµŃé2 | ŹµŃé3 | ŹµŃé4 | ŹµŃé5 | |
| ¼ÓČėŹŌ¼Į0.5mL | Ė® | 5%NaClČÜŅŗ | 5%Mg£ØNO3£©2ČÜŅŗ | 5%FeSO4ČÜŅŗ | 5%CuSO4ČÜŅŗ |
| ²śÉśĘųÅŻĖŁĀŹ | + | + | + | ++ | +++ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 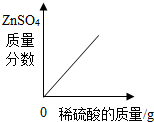 ĻņŅ»¶ØĮæŠæĮ£ÖŠ¼ÓČė¹żĮæĻ”ĮņĖį ĻņŅ»¶ØĮæŠæĮ£ÖŠ¼ÓČė¹żĮæĻ”ĮņĖį | |
| B£® |  ĻņŅ»¶ØĮæĀČ»ÆÄʱ„ŗĶČÜŅŗÖŠ²»¶Ļ¼ÓČėĖ® ĻņŅ»¶ØĮæĀČ»ÆÄʱ„ŗĶČÜŅŗÖŠ²»¶Ļ¼ÓČėĖ® | |
| C£® | 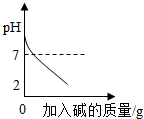 ĻņpH=2µÄČÜŅŗÖŠ¼ÓČė¼īŠŌČÜŅŗ ĻņpH=2µÄČÜŅŗÖŠ¼ÓČė¼īŠŌČÜŅŗ | |
| D£® |  ĻņŅ»¶ØĮæĒāŃõ»ÆÄĘŗĶĢ¼ĖįÄʵĻģŗĻČÜŅŗÖŠ¼ÓČėĻ”ŃĪĖį ĻņŅ»¶ØĮæĒāŃõ»ÆÄĘŗĶĢ¼ĖįÄʵĻģŗĻČÜŅŗÖŠ¼ÓČėĻ”ŃĪĖį |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
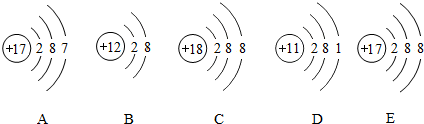
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com