
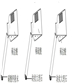
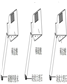
| 实验 操作 |
 |
 |
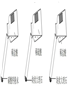 |
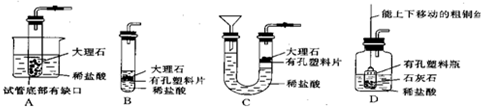
| 现象 | 剧烈反应,产生大量气泡,反应迅速停止 | 产生气泡,速率迅速减慢,反应几乎停止. | 产生气泡,反应持续时间较长 |
| 分析 | 反应速率过快,气体不便收集 | 无法持续产生CO2 | 反应速率适中,可持续产生CO2,便于收集 反应速率适中,可持续产生CO2,便于收集 |
| 结论 | 实验室制取二氧化碳的原料是 块状大理石和稀盐酸 块状大理石和稀盐酸 . | ||
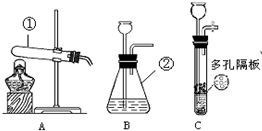
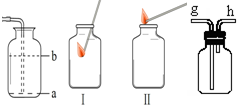
| 比较项目 | 排水集气法 | 向上排空气集气法 |
| 收集方法可行性分析 | CO2生成和从水中逸出速率远大于其溶解速率和与水反应速率 | CO2密度比空气大,且 不与空气反应 不与空气反应 . |
| 收集过程分析 | 集满现象: 集气瓶口有气泡冒出 集气瓶口有气泡冒出 |
“验满”分析:即便燃着木条熄灭,也难以确定空气完全排尽 |
| 向收集到的CO2中倒入等体积石灰水,振荡 | 先浑浊后变澄清所需时间较短 | 先浑浊后变澄清所需时间较长 |
| 由此得出结论 | ① 能 能 (填“能”或“不能”)用排水法收集CO2②用排水法收集的CO2纯度 高 高 (填“高”或“低”) | |
| 不与空气发生反应 | ||
| 集气瓶口有气泡冒出 | ||
| ①能;②高 | ||
| 100 |
| x75% |
| 44 |
| 3.3g |


 活力课时同步练习册系列答案
活力课时同步练习册系列答案科目:初中化学 来源: 题型:
| 实验 步骤 |
 |
 |
 |
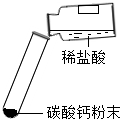
| 现象 | 剧烈反应,产生大量气泡,反应迅速停止 | 产生气泡,速率迅速减慢,反应几乎停止. | 产生气泡,反应持续时间较长 |
| 分析 | 反应速率过快,气体不便收集 | 无法持续产生CO2 | 速率适中,便于收集气体 速率适中,便于收集气体 |
| 结论 | 实验室制取二氧化碳的原料是 块状大理石和稀盐酸 块状大理石和稀盐酸 . | ||
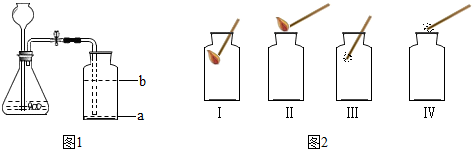
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
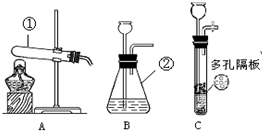
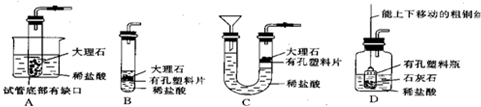
| 实验 操作 | 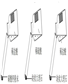 | 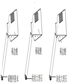 | 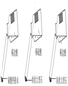 |
| 现象 | 剧烈反应,产生大量气泡,反应迅速停止 | 产生气泡,速率迅速减慢,反应几乎停止. | 产生气泡,反应持续时间较长 |
| 分析 | 反应速率过快,气体不便收集 | 无法持续产生CO2 | ________ |
| 结论 | 实验室制取二氧化碳的原料是________. | ||
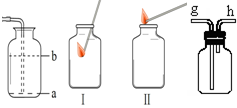
| 比较项目 | 排水集气法 | 向上排空气集气法 |
| 收集方法可行性分析 | CO2生成和从水中逸出速率远大于其溶解速率和与水反应速率 | CO2密度比空气大,且________. |
| 收集过程分析 | 集满现象:________ | “验满”分析:即便燃着木条熄灭,也难以确定空气完全排尽 |
| 向收集到的CO2中倒入等体积石灰水,振荡 | 先浑浊后变澄清所需时间较短 | 先浑浊后变澄清所需时间较长 |
| 由此得出结论 | ①________(填“能”或“不能”)用排水法收集CO2 ②用排水法收集的CO2纯度________(填“高”或“低”) | |
查看答案和解析>>
科目:初中化学 来源:虹口区一模 题型:问答题
| 实验 步骤 |
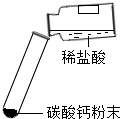 |
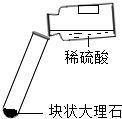 |
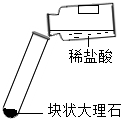 |
| 现象 | 剧烈反应,产生大量气泡,反应迅速停止 | 产生气泡,速率迅速减慢,反应几乎停止. | 产生气泡,反应持续时间较长 |
| 分析 | 反应速率过快,气体不便收集 | 无法持续产生CO2 | ______ |
| 结论 | 实验室制取二氧化碳的原料是______. | ||
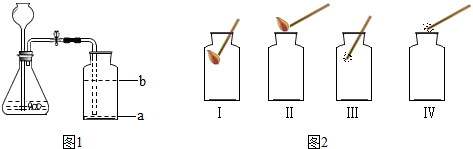
查看答案和解析>>
科目:初中化学 来源:2012-2013学年江苏省扬州市仪征市大仪中学九年级(上)期中化学试卷(解析版) 题型:解答题
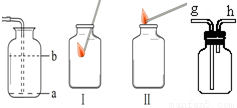
| 实验 操作 |  |  | 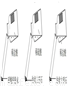 |
| 现象 | 剧烈反应,产生大量气泡,反应迅速停止 | 产生气泡,速率迅速减慢,反应几乎停止. | 产生气泡,反应持续时间较长 |
| 分析 | 反应速率过快,气体不便收集 | 无法持续产生CO2 | ______ |
| 结论 | 实验室制取二氧化碳的原料是______. | ||
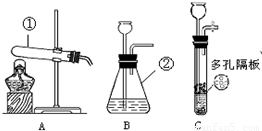

| 比较项目 | 排水集气法 | 向上排空气集气法 |
| 收集方法可行性分析 | CO2生成和从水中逸出速率远大于其溶解速率和与水反应速率 | CO2密度比空气大,且______. |
| 收集过程分析 | 集满现象:______ | “验满”分析:即便燃着木条熄灭,也难以确定空气完全排尽 |
| 向收集到的CO2中倒入等体积石灰水,振荡 | 先浑浊后变澄清所需时间较短 | 先浑浊后变澄清所需时间较长 |
| 由此得出结论 | ①______(填“能”或“不能”)用排水法收集CO2 ②用排水法收集的CO2纯度______(填“高”或“低”) | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com