
| 实验次数 | 加入稀盐酸的质量/g | 剩余固体的质量/g |
| 1 | 10 | 8 |
| 2 | 10 | 6 |
| 3 | 10 | 4 |
| 4 | 10 | 2 |
| 5 | 10 | 2 |
分析 (1)根据每次加入10g的盐酸后,固体质量都减少2g,依据表中的数据进行分析;
(2)根据石灰石样品中的杂质不参与反应,也不溶于水,最后剩余固体的质量就是杂质的质量进行分析;
(3)根据固体减少的质量就是碳酸钙的质量,依据化学方程式进行计算.
解答 解:(1)通过分析表中的数据可知,第4加入稀盐酸充分反应,CaCO3恰好完全反应;
(2)石灰石样品中CaCO3的质量分数为:$\frac{10g-2g}{10g}$×100%=80%;
(3)设盐酸的质量分数为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73
2g 10g×x
$\frac{100}{2g}$=$\frac{73}{10g×x}$
x=14.6%
故答案为:(1)4;
(2)石灰石样品中CaCO3的质量分数为80%;
(3)盐酸的质量分数为14.6%.
点评 本题主要考查了化学方程式的计算,难度不大,注意解题的规范性和准确性.


科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前的质量(g) | 7.6 | 2.0 | 0.2 | 0 |
| 反应后的质量(g) | 3.2 | X | 5.8 | 0.4 |
| A. | X=0.4 | |
| B. | 丁一定是单质 | |
| C. | 甲和乙是反应物 | |
| D. | 反应中的甲、丙发生改变的质量比是11:14 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
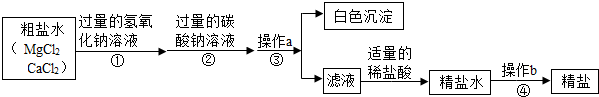
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

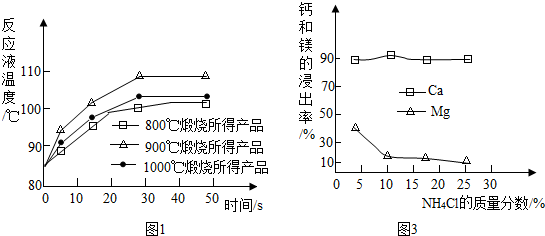
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 名称 | 主要成分 |
| 雪碧 | 碳水化合物、水 |
| 苏打水(弱碱性) | 碳酸氢钠、水 |
| 盐汽水 | 氯化钠、水 |
| 柠檬汁 | 水、碳水化合物、蛋白质、纤维、维生素等 |
| A. | 雪碧是一种混合物 | |
| B. | 4种饮料中,苏打水的pH值最小 | |
| C. | 从事高温作业的人员,适宜补充盐汽水 | |
| D. | 喝适量柠檬汁有助于补充人体的维生素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com