
| A. | 分子是不断运动的 | B. | 分子是可分的 | ||
| C. | 品红分子发生变化 | D. | 分子体积极小 |
分析 根据分子的基本特征:分子质量和体积都很小;分子之间有间隔;分子是在不断运动的;同种物质的分子性质相同,不同物质的分子性质不同,可以简记为:“两小运间,同同不不”,结合事实进行分析判断即可.
解答 解:向盛有水的烧杯中加人少量品红,品红在静置的水中扩散,是因为品红中含有的分子是在不断的运动的,向四周扩散.
A、由于分子是在不断的运动的,这是造成品红在静置的水中扩散的主要原因,故选项正确.
B、由分子的性质可知,品红在静置的水中扩散的主要原因与分子可分无关,故选项错误.
C、由分子的性质可知,品红在静置的水中扩散的主要原因与品红分子是否发生了变化无关,故选项错误.
D、由分子的性质可知,品红在静置的水中扩散的主要原因与分子的体积大小无关,故选项错误.
故选:A.
点评 本题难度不大,掌握分子的基本性质(可以简记为:“两小运间,同同不不”)及利用分子的基本性质分析和解决问题的方法是解答此类题的关键.


 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:初中化学 来源: 题型:选择题

| A. | E转化为B不一定是置换反应 | |
| B. | D、F中相同元素的化合价一定不相同 | |
| C. | E一定是氧化铜 | |
| D. | 若A由3种元素组成,则A的化学式一定是CaCO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
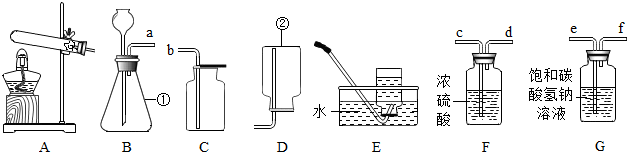
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
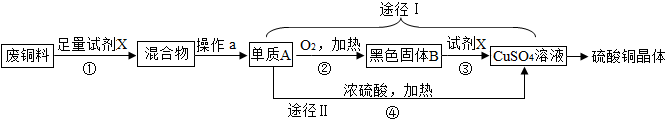
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 胃液 | 胆汁 | 血浆 | 胰液 |
| 0.9~1.5 | 7.1~7.3 | 7.35~7.45 | 7.5~8.0 |
| A. | 胃液 | B. | 胆汁 | C. | 血浆 | D. | 胰液 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
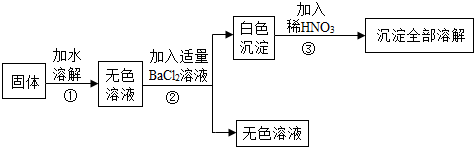
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 内容 装置 | 实验1制备气体 | 实验2测定气体含量 |
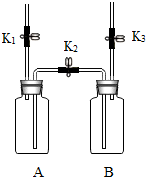 | Ⅰ.打开K1,用注射器向盛有锌粒的A中注入稀硫酸,直至液面浸没下端导管口 Ⅱ.在K1上方导管口收集气体 | Ⅰ.A(容积350mL)中为用排空气法收集的二氧化碳,B中装满水.用注射器向A中注入15mL NaOH溶液(足量),充分反应 Ⅱ.打开K2和K3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com