
【题目】某厂电镀液废水中含有硫酸和硫酸铜两种溶质为测定其中各成分的含量,69 中化学实验小组的同学们取 100g 废水样品,在实验室中利用溶质质量分数为 20% 的 NaOH 溶液进行测定,所得到的相关数据如图所示。请回答下列问题:
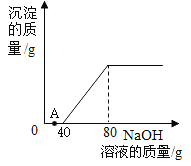
(1)A 点发生反应的化学方程式为______________;
(2)根据已知条件,列出求解反应生成沉淀的质量(x)的比例式为________________;
(3)A 点溶液中含有的离子是_________________(填离子符号) ;
(4)当加入 80g 氢氧化钠溶液充分反应后过滤出沉淀,将溶液蒸发掉 28.2g 水,所得到的不饱和溶液中溶质的质量分数为______________;
(5)若想把 100kg 这样的废液转化为纯净的硫酸铜溶液,需要加入含杂质 20%的氧化铜(杂质不溶于水,也不与酸反应)的质量为______________。再经过一系列操作,就可以得到纯净的硫酸铜溶液。
【答案】![]()
![]() H+、SO42-、Na+ 20% 10kg
H+、SO42-、Na+ 20% 10kg
【解析】
(1)向废水样品中加入氢氧化钠溶液,氢氧化钠先与硫酸反应生成硫酸钠和水,待硫酸完全反应后,氢氧化钠再与硫酸铜反应生成氢氧化铜和硫酸钠,由图可知,A点时,无沉淀产生,故是氢氧化钠与硫酸反应生成了硫酸钠和水,该反应的化学方程式为:![]() ;
;
(2)由图可知,加入氢氧化钠溶液的质量为80g时,沉淀质量不再变化,故这时,氢氧化钠与硫酸铜恰好完全反应,硫酸铜消耗氢氧化钠的质量为:(80g-40g)×20%=8g;
解:设生成沉淀的质量为x,反应生成硫酸钠的质量为y
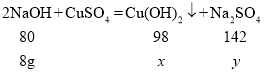
![]() x=9.8g
x=9.8g
![]() y=14.2g
y=14.2g
答:求解反应生成沉淀的质量(x)的比例式为:![]() ;
;
(3)氢氧化钠与硫酸反应生成硫酸钠和水,A点时,硫酸未完全反应,故A 点溶液中含有的离子是:H+、SO42-、Na+;
(4)解:设氢氧化钠与硫酸反应生成硫酸钠的质量为z,废水中硫酸的质量分数为m

![]() z=14.2g
z=14.2g
![]() m=9.8%
m=9.8%
所得到的不饱和溶液中溶质的质量分数为:![]() ;
;
(5)解:设需要含杂质20%的氧化铜的质量为n

![]() n=10kg
n=10kg
答:需要含杂质20%的氧化铜的质量为10kg。


科目:初中化学 来源: 题型:
【题目】进行如图实验,研究物质的性质。
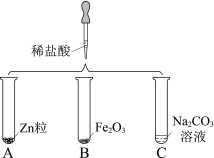
(1)A中的现象是______。
(2)B中反应的化学方程式为______。
(3)C中滴入稀盐酸后得到溶液甲,向甲中继续滴加Ca(OH)2溶液,有白色沉淀生成。溶液甲中的溶质是______(填化学式)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2019 年12月以来,部分地区突发的新型冠状病毒肺炎威胁着人们的身体健康。预防病毒除了戴口罩、勤洗手,还要做好消毒工作。市面上可以有效消灭新型冠状病毒的消毒剂如下图所示:
医用酒精: 75%的乙醇溶液,
84消毒液: >0.05%的次氯酸钠溶液等,
医用消毒液:过氧化氢过氧乙酸消毒液
衣服消毒液: >0.12%的对氯间二甲苯酚
季铵盐溶液:>0.2%季铵盐溶液
请按要求填空:
①将部分消毒剂中的主要成分进行分类(选填“有机物、酸、碱、盐、氧化物”)
物质 | 酒精 | 次氯酸钠(NaClO) | 过氧化氢 |
物质类别 | ___ | ___ | ___ |
②使用医用酒精进行消毒时,要远离明火,这是因为酒精具有___的化学性质。
③公共场合可用0.5%的过氧乙酸(化学式为C2H4O3)溶液进行消毒。过氧乙酸的摩尔质量为______, 1摩尔过氧乙酸中碳原子的个数为_______个(用科学计数法)。若要配制这样的溶液1000克,需要过氧乙酸___克。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】侯德榜制碱法的原理是:向氨化的饱和食盐水中通入过量的二氧化碳,即有晶体析出,经过滤、洗涤、焙烧得纯碱.此过程可以表示为:①![]() (此反应是放热反应) ②煅烧碳酸氢钠后,得到纯碱。侯氏制碱法生产流程示意图:
(此反应是放热反应) ②煅烧碳酸氢钠后,得到纯碱。侯氏制碱法生产流程示意图:

[查阅资料]I.氨化的饱和食盐水;即是指向饱和食盐水中通入氨气;Ⅱ.NaHCO3低温时溶解度很小; III在通常状况下,NH3极易溶于水,CO2能溶于水。
(1)请你填写出括号中物质的化学式_____________。
(2)用化学方程式表达煅烧炉中发生的反应___________。
(3)向饱和的食盐水中,先通入氨气再通人二氧化碳的目的是____________。
(4)向母液中通入氨气的原因是___________;把母液冷却至10°C以下的目的是________。
(5)侯氏制碱法的生产流程中,可以循环利用的物质是____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是一氧化碳与氧气反应的微观模拟图,请回答下列问题:

(1)在乙、丙图中将相关粒子图形补充完整____________;
(2)该反应的基本反应类型是_____________,你判断的微观依据是_____________;
(3)画出比氧原子多一个周期少一个族的原子结构示意图_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下表是Ca(OH)2和NaOH的溶解度数据。请回答下列问题:
温度/°C | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度/(g/100g水) | Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
NaOH | 31 | 91 | 111 | 129 | 313 | 336 | |
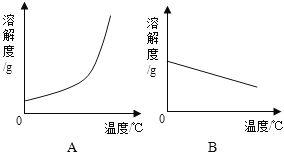
①依据上表数据,绘制Ca(OH)2和NaOH的溶解度曲线,下图中表示NaOH溶解度曲线的是_____(填A或B)。
②把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,具体措施有_____。(填一种)
③20℃时,191g饱和NaOH溶液,恒温蒸发10g水后,可析出NaOH晶体_____g。
④现有60°C时含Ca(OH)2和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH晶体,应采取的物理方法是_____。
⑤20℃时,欲测定NaOH溶液的pH,若先将pH试纸用蒸馏水润湿,再进行测定,则所测溶液的pH_____(填“偏大”、“偏小”或“不受影响”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用辉铜矿(主要成分为Cu2S,含少量Fe2O3、SiO2等杂质)制备难溶于水的碱式碳酸铜的流程如下:
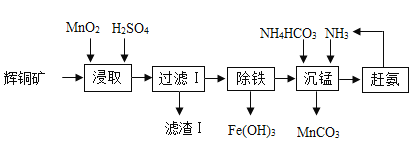
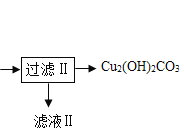
(1)请写出碱式碳酸铜的化学式_____
(2)滤渣l中有什么_____
(3)过滤用到到仪器有那些_____
(4)除铁的化学方程式是什么_____
(5)图中能重复利用的物质有那些_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙两种固体物质的溶解度曲线如图所示。下列说法正确的是
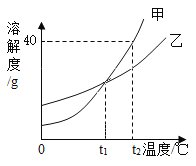
A.t1℃时,甲、乙的饱和溶液中溶质的质量相等
B.t2℃时,甲的饱和溶液中溶质和溶液的质量比为2:5
C.t2℃时,将等质量的甲乙配制成该温度下的饱和溶液,所得溶液的质量甲>乙
D.分别将甲、乙的饱和溶液从t2℃降温到t1℃,所得溶液中溶质质量分数相等
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】归纳与演绎是重要的科学方法,也常用于化学的学习。请根据下列实验装置,回答问题:

(1)装置B中反应的方程式为_____。要随时使反应停止或发生,可选择的发生装置有_____(填序号,从A﹣E中选择)。若用E和G组装一套气密性好的装置来测定二氧化碳的体积,反应结束后,发现量筒内收集到的水的体积总是比理论值偏小,原因是二氧化碳_____。
(2)若用双氧水和二氧化锰制取氧气且能获得平稳的气流,可选择的发生装置有_____(填序号),方程式是_____。
(3)化学上可通过多种反应得到氨气(极易溶于水,密度比空气小),例如:
①氯化铵(固)+氢氧化钙(固)![]() 氯化钙+氨气+水
氯化钙+氨气+水
②碳酸氢铵(固)![]() 氨气+二氧化碳+水
氨气+二氧化碳+水
结合以上实验装置完成下列填空:你选择上述反应_____(填序号)作为实验室制取氨气的反应原理,选用上图中A~H的_____(填序号)作为反应的发生装置,采用的收集装置是F和H,其中氨气应从_____(填a或b)管导入F中,选用的H装置,其实是作为尾气处理的,其中采用的倒置的漏斗,目的是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com