水是生命之源,没有水就没有生命,小明对他所住村庄的井水含有什么成分非常感兴趣,于是他做了如下探究:
[提出问题]井水是酸性的、碱性的、还是中性的?
[探 究 一]①小明用玻璃棒蘸取少量井水,滴在PH试纸上.
[现 象]井水的PH大约为6.
[反 思]小明的实验操作无误,为什么井水的PH会小于7呢?认为可能的原因是________.
[提出问题]井水是硬水还是软水?
[探 究 二]②小明取20mL井水放入一个小烧杯中,然后加入________,搅拌.
[现 象]有少许泡沫,有较多的浮渣.
[结 论]该井水是________水.
[提出问题]③小明家烧开水的水壶底部厚厚的水垢,水垢的主要成分是什?
[探 究 三]小明取一些水垢放入大试管中,加入足量的食醋.
[现 象]固体溶解,并放出一种使澄清石灰水变浑浊的气体.
[结 论]水垢中的主要成分是________.
[反思与拓展]④井水是无色透明的,为什么烧开水后能形成水垢呢?说明水中应该含有________.写出加热过程中形成水垢主要成分的化学方程式:________.
经过这次实验之后,小明改变了吃生水的习惯.
水中溶有空气中二氧化碳 肥皂水 硬 碳酸钙 可溶性钙镁化合物 Ca(HCO3)2?CaCO3↓+H2O+CO2↑
分析:①井水的PH会小于7说明显酸性,寻找空气中成分溶于水显酸性的物质即可;
②根据硬水与软水鉴别方法来回答本题;
③根据碳酸根的鉴别方法入手;
④由加热过程中形成水垢碳酸钙,再结合学过去的知识会联想到碳酸氢钙受热分解.
解答:解;①由于空气中二氧化碳能溶于水,生成碳酸属于酸使井水的PH大约为6;
②鉴别硬水和软水的方法是用肥皂水,加入肥皂水后泡沫多的是软水,泡沫少且有浮渣的是硬水;
③加入酸能产生二氧化碳说明该物质中含有碳酸根离子,又因为是硬水,所以水垢中的主要成分是碳酸钙;
④因为水垢的主要成分是碳酸钙,说明水中应该含有可溶性钙镁化合物,由于硬水经过煮沸就可软化,所以方程式是碳酸氢钙受热分解.
故答案为:①水中溶有空气中二氧化碳;
②肥皂水,硬;
③碳酸钙;
④可溶性钙镁化合物,Ca(HCO3)2?CaCO3↓+H2O+CO2↑.
点评:掌握软水与硬水的区别和联系,鉴别方法,硬水软化的方法,了解清除水壶中水垢的方法.



 水是生命之源,人类的日常生活与工农业生产都离不开水.
水是生命之源,人类的日常生活与工农业生产都离不开水.
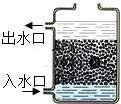
 (2)如图是市场上出售的一种活性炭净水器示意图.这种净水器入水口在下方的优点是
(2)如图是市场上出售的一种活性炭净水器示意图.这种净水器入水口在下方的优点是 “水是生命之源,没有水就没有生命”.去年冬天至今年春天,我国西南地区遭遇大范围持续干旱.全国人民团结一致,共同抗旱.请根据所学知识回答下列问题:
“水是生命之源,没有水就没有生命”.去年冬天至今年春天,我国西南地区遭遇大范围持续干旱.全国人民团结一致,共同抗旱.请根据所学知识回答下列问题: 水是生命之源,没有水就没有生命.
水是生命之源,没有水就没有生命.
