
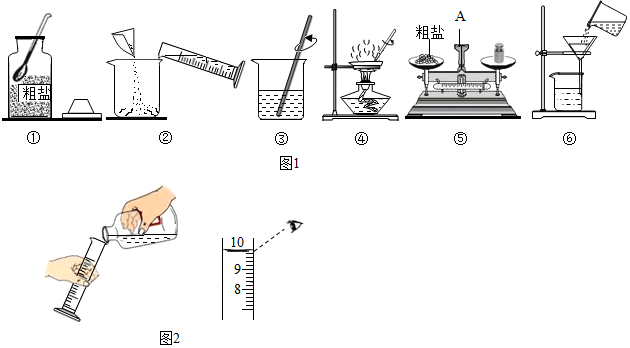
分析 (1)根据实验室常用仪器的名称和题中所指仪器的主要进行分析;
(2)根据过滤时应该用玻璃棒引流进行分析;
(3)根据固体溶解过程中,玻璃棒的作用是:搅拌,加速固体溶解进行分析;
(4)根据粗盐提纯实验的操作顺序为:取出药品,称量,把粗盐和水转移到烧杯中溶解,过滤,蒸发进行分析;
(5)根据镁离子用氢氧根离子沉淀,硫酸根离子用钡离子沉淀,钙离子用碳酸根离子沉淀,过滤要放在所有的沉淀操作之后,加碳酸钠要放在加氯化钡之后,可以将过量的钡离子沉淀最后再用盐酸处理溶液中的碳酸根离子和氢氧根离子进行分析;
(6)根据俯视读数时,水的实际体积小于所读数据的体积进行分析.
解答 解:(1)通过分析题中所指仪器的作用可知,A是托盘天平;
(2)操作⑥中的错误是没用玻璃棒引流;
(3)固体溶解过程中,玻璃棒的作用是:搅拌,加速固体溶解;
(4)粗盐提纯实验的操作顺序为:取出药品,称量,把粗盐和水转移到烧杯中,加入水搅拌溶解,再过滤,蒸发即可得到精盐,所以粗盐提纯实验的操作顺序为:①⑤②③⑥④;
(5)镁离子用氢氧根离子沉淀,加入过量的氢氧化钠可以将镁离子沉淀,硫酸根离子用钡离子沉淀,加入过量的氯化钡可以将硫酸根离子沉淀,至于先除镁离子,还是先除硫酸根离子都行,钙离子用碳酸根离子沉淀,除钙离子加入碳酸钠转化为沉淀,但是加入的碳酸钠要放在加入的氯化钡之后,这样碳酸钠会除去反应剩余的氯化钡,离子都沉淀了,再进行过滤,最后再加入盐酸除去反应剩余的氢氧根离子和碳酸根离子,所以正确的顺序为:加过量的BaCl2溶液,加过量的Na2CO3溶液,加过量的NaOH溶液,过滤,加适量的盐酸;或者,加过量的NaOH溶液,加过量的BaCl2溶液,加过量的Na2CO3溶液,过滤,加适量的盐酸或加过量的BaCl2溶液,加过量的NaOH溶液,加过量的Na2CO3溶液,过滤,加适量的盐酸;所以操作顺序为:③⑥⑤①④②,加过量的Na2CO3溶液的目的是:除去氯化钙和过量的氯化钡;
(6)俯视读数时,水的实际体积小于所读数据的体积,所以配制一定量5%的NaCl溶液时,所配制溶液的溶质质量分数偏大.
故答案为:(1)托盘天平;
(2)没用玻璃棒引流;
(3)搅拌,加速固体溶解;
(4)①⑤②③⑥④;
(5)③⑥⑤①④②,除去氯化钙和过量的氯化钡;
(6)偏大.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | 图①表示室温下,向不饱和硝酸钾溶液中加入硝酸钾 | |
| B. | 图②表示在 AgNO3和 Cu(NO3)2的混合溶液中加入铁粉 | |
| C. | 图③表示两份质量和浓度都相同的 H2O2溶液产生 O2的质量与时间 t的关系 | |
| D. | 图④表示向相等质量的镁、铝、锌、铁四种金属中,加入足量的稀盐酸 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com