
ij��ȤС��ͬѧΪ֤��NaOH��Һ��ϡ���ᷢ�����кͷ�Ӧ���Ӳ�ͬ�Ƕ����������ʵ�鷽����������ʵ�顣
����һ������pH��ֽ�ⶨNaOH��Һ��pH���ٵμ����ᣬ����������Һ��ͬʱ�ⶨ�����Һ��pH�������õ�pH��С��С��7����֤��NaOH��Һ��ϡ���ᷢ���˻�ѧ��Ӧ��
(1)��pH��ֽ�ⶨ��Һ��pHʱ����ȷ�IJ����ǣ�
����2�֣�
(2)����ǿ������õ�pHС��7�������ɣ� ��
������������NaOH��Һ�еμӼ��η�̪��Һ����Һ�Ժ�ɫ��Ȼ���ٵμ����ᣬ�ɹ۲쵽��ɫ����ʧ����֤��NaOH��Һ��ϡ���ᷢ���˻�ѧ��Ӧ��
����ͬѧ����NaOH��Һ�еμӷ�̪��Һʱ��������һ��������������������Һ�е����̪��Һ����Һ����˺�ɫ������һ�����ɫ����ʧ�ˡ���С����������������ԭ���������²��룺�ٿ����Ƿ�̪��Һ������е�������Ӧ��ʹ��ɫ��ʧ��
�ڿ���������������Һ������еĶ�����̼��Ӧ��ʹ��ɫ��ʧ��
(1)Ϊ��֤����٣�����ͬѧ��������ʵ�飺�����Ƶ�����������Һ���ȣ�����Һ���Ϸ���һЩֲ���ͣ�Ȼ������ȴ�����Һ�е����̪��Һ��ʵ���С����ȡ��͡�����ֲ���͡�Ŀ���� ��ʵ����������̪��Һ��ɫ��ʧ������е������ء�
(2)Ϊ��֤����ڣ�����ͬѧ��������ʵ�飺ȡ��һ������Na2CO3��Һ�������е����̪��Һ��������ҺҲ���ֺ�ɫ���ɴ˿ɵó�����������ۣ�
����1��˵��Na2CO3��Һ�� �ԣ�
����2��˵����̪��Һ��ɫ��ʧ������еĶ�����̼�ء�
(3)��С��ͬѧͨ���������ϵ�֪��������������ҺŨ�Ⱥܴ�ʱ���ͻ���������������������ʵ��֤���÷�����ȡ�õ�NaOH��ҺŨ�ȹ���ʵ�鷽��
���ڹ۲쵽������ ��
����������ѧ��Ӧ��ͨ�������������ı仯���ɽ�����Ӧǰ����¶ȱ仯���жϷ�Ӧ�ķ��������NaOH��Һ��ϡ������ǰ���¶��б仯����֤�������˻�ѧ��Ӧ��
����ͬѧ����ͬŨ�ȵ������NaOH��Һ��10 mL��ϣ����¶ȼƲⶨ�����»��ǰ���¶ȵı仯������¼��ÿ�λ��ǰ���¶ȵ�����ֵ��t�����±�����
| ��� | ���� | NaOH��Һ | ��t/�� |
| 1 | 3.65﹪ | 2.00﹪ | 3.5 |
| 2 | 3.65﹪ | 4.00﹪ | x |
| 3 | 7.30﹪ | 8.00﹪ | 14 |
(1)����x = ��
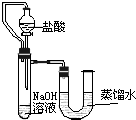
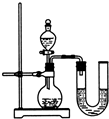
(2)ijͬѧ��ûʹ���¶ȼƵ�����£�ͨ����ͼ��ʾװ�������ʵ�顣���ͬѧ����
�ж�NaOH��Һ��ϡ���ᷢ�����кͷ�Ӧ��

�ǹ���ʵ���е�ϸ�ں����������
��ʵ���У�ϡ��������ý�ͷ�ι���εμӣ���������Ŀ���� ��
��ʵ������У�Ҫ�ò��������Ͻ��裬��������Ŀ���� ��
����ʵ����������ⷢ�������ݳ��֣�����Ϊԭ���� ��
�ܷ���ʢ��NaOH��Һ���Լ�ƿƿ�ں���Ƥ���ϳ����˰�ɫ��ĩ������������ѧ�Ļ�ѧ֪ʶ�������ְ�ɫ��ĩ�ijɷ��������²��룺�� ������NaOH������Ϊ���� ������__________�� �� ������_________________________��
��Ϊ�˽�һ���о�ʵ���г��ֵ����⣬
ȡ��13.3g�������ƹ�����Ʒ��������ˮ�����Һ�������м���200g10%��ϡ���ᣬʹ���ַ�Ӧ�����ɶ�����̼2.2g����
����Ʒ���������Ƶ�������
�ƺ��������Ʒ�Ӧ�������������
������ͼ�л������������ʾ������̼�������������ʾ����������Ĺ�ϵͼ������֪Na2CO3 +2HCl === 2NaCl + H2O+CO2����
 |
����һ�� (1) ��PH��ֽ���ڱ������ϣ��ò�����պȡ��������Һ������ֽ�ϣ�����ֽ��ɫ���ɫ�����ն���pH����2�֣�(2) �ų���ϡ�Ͷ�ʹ��ҺpH��С������ ��
�������� (1) �������� ��(2) �� ��
(3) ȡ������Һ��ˮϡ�ͺ��ٵμ���ɫ��̪ ���� ��Һ�ʺ�ɫ ��
�������� (1) 7 ��(2)U����Һ������Ҹ�
�� �� ��ֹϡ������� �� ʹ��Ӧ��� �� ����������Һ�к���̼����
1�� ��Na2CO3 NaOH��Na2CO3�Ļ����
�Ƚ⣺�������Ʒ��̼���Ƶ�����Ϊx����̼���Ʒ�Ӧ�����������Ϊy��1�֣�
Na2CO3 +2HCl === 2NaCl + H2O+CO2�� ��0.5�֣�
 106 73 44
106 73 44
x y��10% 2.2g
106��x=73����y��10%��=44��2.2g ��1�֣�
x=5.3g y=36.5g
NaOH������Ϊ��13.3g-5.3g=8g ��2�֣�
����������Ʒ�Ӧ�����������Ϊz
NaOH+ HCl === NaCl + H2O ��0.5�֣�
40 36.5
8g z ��10% 40��36.5=8g����z��10%�� ��1�֣� z=73g ��1�֣�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ��� | ���� | NaOH��Һ | ��t/�� |
| 1 | 3.65% | 2.00% | 3.5 |
| 2 | 3.65% | 4.00% | x |
| 3 | 7.30% | 8.00% | 14 |
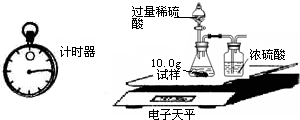
| �� �� �� Ŀ | �� �� ʱ �� | ������g�� |
| ���� | 10.00 | |
| װ��+ϡ�������� | 241.20 | |
| װ��+ϡ��������+���� | ��Ӧ��ʼ��15�� | 249.20 |
| װ��+ϡ��������+���� | ��Ӧ��ʼ��35�� | 249.00 |
| װ��+ϡ��������+���� | ��Ӧ��ʼ��55�� | 249.00 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
 ����֮�䷢����ѧ��Ӧʱ�������������Ե�������Щ��ѧ��Ӧȴ�۲첻�����Ե�����ij��ȤС��ͬѧΪ֤��NaOH��Һ��ϡ���ᷢ�����кͷ�Ӧ���Ӳ�ͬ�Ƕ����������ʵ�鷽����������ʵ�飮
����֮�䷢����ѧ��Ӧʱ�������������Ե�������Щ��ѧ��Ӧȴ�۲첻�����Ե�����ij��ȤС��ͬѧΪ֤��NaOH��Һ��ϡ���ᷢ�����кͷ�Ӧ���Ӳ�ͬ�Ƕ����������ʵ�鷽����������ʵ�飮| ��� | ���� | NaOH��Һ | ��t�� |
| 1 | 3.65% | 2.00% | 3.5 |
| 2 | 3.65% | 4.00% | |
| 3 | 7.30% | 8.00% | 14 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com