

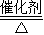
 2KCl+3O2↑
2KCl+3O2↑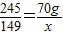 x=42.6g
x=42.6g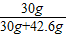 ×100%=41.3%
×100%=41.3%

科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
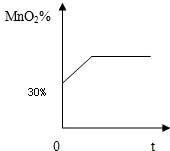 实验室用加热氯酸钾与二氧化锰混合物的方法来制取氧气,在制取过程中,固体中二氧化锰的质量分数(MnO2%)随加热时间(t)的变化情况如图.当二氧化锰的质量分数为多少时不再产生氧气( )
实验室用加热氯酸钾与二氧化锰混合物的方法来制取氧气,在制取过程中,固体中二氧化锰的质量分数(MnO2%)随加热时间(t)的变化情况如图.当二氧化锰的质量分数为多少时不再产生氧气( )| A、37.6% | B、42.2% | C、41.3% | D、53.8% |
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
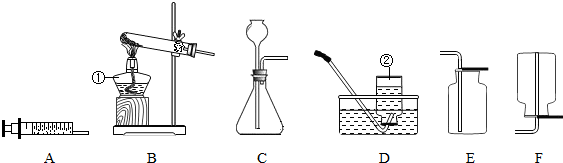
| 二氧化锰 |
| 加热 |
| 二氧化锰 |
| 加热 |
| 实验编号 | 实验药品 | 分解温度(℃) |
| ① | KCl03 | 580 |
| ② | KCl03、Mn02(质量比1:1) | 350 |
| ③ | KCl03、CuO(质量比l:1) | 370 |
| ④ | KCl03、Fe203(质量比1:1) | 390 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
| △ |
| ||
| △ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com