已知尿素CO(NH2)2和硝酸铵NH4NO3.
①计算尿素的相对分子质量.
②计算NH4NO3中各元素质量比.
③100克硝酸铵中所含氮元素质量与多少尿素所含氮元素质量相等?
解:(1)根据尿素的化学式可知,它的相对分子质量=12+16+14×2+1×4=60;
(2)硝酸铵氮、氢、氧元素的质量比=(14×2):(1×4):(16×3)=7:1:12;
(3)100kg硝酸铵中含氮质量=100kg×
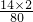
=35kg,
含35kg氮元素的尿素质量=35kg÷
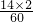
=75kg.
答:(1)尿素的相对分子质量为60;
(2)硝酸铵中氮、氢、氧元素的质量比为7:1:12;
(3)75千克尿素[CO(NH
2)
2]所含氮元素的质量与100kg硝酸铵的含氮质量相等.
分析:(1)根据尿素的化学式可知,尿素的相对分子质量=(碳的相对原子质量×碳原子个数)+(氧的相对原子质量×氧原子个数)+(氮的相对原子质量×氮原子个数)+(氢的相对原子质量×氢原子个数);
(2)硝酸铵中各元素的质量比N:H:O=(氮的相对原子质量×氮原子个数):(氢的相对原子质量×氢原子个数):(氧的相对原子质量×氧原子个数);
(3)根据“100kg×硝酸铵的含氮量÷尿素[CO(NH
2)
2]所含氮元素的质量分数”计算.
点评:本题主要考查学生运用化学式进行计算的能力,解题时要注意计算物质中元素的质量比时要写出元素的顺序.

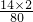 =35kg,
=35kg,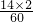 =75kg.
=75kg.
