
 某化学兴趣小组的同学进行了以下实验:向烧杯中加入变质的氢氧化钙固体和一定量的稀盐酸,一段时间后固体全溶解.他们对所得溶液中的溶质成分进行了探究.
某化学兴趣小组的同学进行了以下实验:向烧杯中加入变质的氢氧化钙固体和一定量的稀盐酸,一段时间后固体全溶解.他们对所得溶液中的溶质成分进行了探究.分析 Ⅰ、【猜想】根据反应的程度进行猜想:恰好反应、一种物质完全反应,另一种物质有剩余进行解答;
【进行实验】根据酚酞遇碱变红、碳酸钠溶液能和盐酸反应放出二氧化碳气体,碳酸钠溶液与氯化钙溶液反应生成碳酸钙沉淀和氯化钠来进行解答;
【反思与拓展】
(1)根据氢氧化钙和二氧化碳反应生成碳酸钙和水进行解答;
(2)根据石灰石或大理石能与盐酸反应进行解答;
Ⅱ(1)根据碳酸钠和盐酸反应生成氯化钠、水和二氧化碳;碳酸钠和氯化钙溶液反应生成碳酸钙沉淀和氯化钠以及碳酸钠溶液呈碱性进行解答;
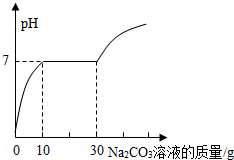
(3)根据图示可知,碳酸钠溶液要先与盐酸反应,从10g开始,加入的碳酸钠溶液才开始与氯化钙溶液反应进行分析.
解答 解:Ⅰ、【猜想】反应可能是恰好反应,只有氯化钙(猜想三)、也可能是一种物质完全反应,另一种物质有剩余,若氢氧化钙过量,则含有氢氧化钙和氯化钙(猜想二);若盐酸过量,则含有盐酸和氯化钙(猜想四);
【进行实验】因为酚酞遇碱会变红色,而结论是猜想二不正确,即不含有氢氧化钙,故观察到的现象是溶液不变红色;碳酸钠溶液能和盐酸反应放出二氧化碳气体,碳酸钠溶液与氯化钙溶液反应生成碳酸钙沉淀和氯化钠,所以另取少量烧杯内溶液与试管中,逐滴加入碳酸钠溶液至过量,先有气体产生,后产生沉淀,说明猜想四正确;
【反思与拓展】
(1)氢氧化钙和二氧化碳反应生成碳酸钙和水,化学方程式为Ca(OH)2+CO2═CaCO3↓+H2O;
(2)石灰石或大理石能与盐酸反应生成氯化钙,所以可用石灰石或大理石处理;
Ⅱ(1)碳酸钠和盐酸反应生成氯化钠、水和二氧化碳;碳酸钠和氯化钙溶液反应生成碳酸钙沉淀和氯化钠,碳酸钠溶液呈碱性,由图示可知,当碳酸钠溶液质量加到10g时,溶液中盐酸恰好反应完;
(3)根据图示可知,碳酸钠溶液要先与盐酸反应,从10g开始,加入的碳酸钠溶液才开始与氯化钙溶液反应.
设氯化钙的质量为x.
氯化钙消耗的碳酸钠的质量=(30g-10g)×5.3%=1.06g
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 111
1.06g x
$\frac{106}{1.06g}=\frac{111}{x}$
x=1.11g
原烧杯溶液中氯化钙的质量分数=$\frac{1.11g}{10g}×100%$=11.1%
答:原烧杯溶液中氯化钙的质量分数为11.1%.
故答案为:【猜想】CaCl2;猜想一;
【进行实验】溶液呈无色;先有气泡产生,后有沉淀产生;
【反思与拓展】(1)Ca(OH)2+CO2═CaCO3↓+H2O;(2)石灰石或大理石;
Ⅱ.(1)10;(2)11.1%.
点评 本题考查了酸碱中和反应以及实验设计的能力.设计实验时,可以从反应后的产物和其有关的性质着手;检验时要注意氯离子的干扰.


科目:初中化学 来源: 题型:填空题
 已知A、B、C为氧化物,D为单质,是初中化学常见的物质,B、D中含有地壳中含量第二的金属元素,它们之间转化关系和反应条件如图:
已知A、B、C为氧化物,D为单质,是初中化学常见的物质,B、D中含有地壳中含量第二的金属元素,它们之间转化关系和反应条件如图:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | BaCuSi2O6中含有3种金属元素 | |
| B. | BaCuSi2O6中硅元素的化合价为+4价 | |
| C. | BaCuSi2O6中钡元素与氧元素的质量比为1:6 | |
| D. | BaCuSi2O6的相对分子质量为245 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
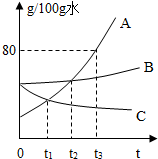 如图是A、B、C三种固体物质的溶解度曲线图.请结合图示回答下列问题:
如图是A、B、C三种固体物质的溶解度曲线图.请结合图示回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 序号 | 待鉴别的物质 | 鉴别试剂或方法 |
| A | 尿素与氯化铵固体 | 熟石灰、研磨 |
| B | 硝酸铵与食盐固体 | 水、溶解 |
| C | 氢氧化钠溶液与碳酸钠溶液 | 酚酞溶液 |
| D | 一氧化碳与二氧化碳气体 | 澄清的石灰水 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 实验室里有一瓶标签残缺的试剂瓶,标签中只剩下“Na”和“10%”字样(如图所示),某兴趣小组对其组成进行如下探究.
实验室里有一瓶标签残缺的试剂瓶,标签中只剩下“Na”和“10%”字样(如图所示),某兴趣小组对其组成进行如下探究.| 物质 | NaHCO3 | NaCl | NaOH | Na2CO3 |
| 溶解度g/100g水 | 9.6 | 36 | 109 | 215 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 该反应可能是复分解反应 | |
| B. | 若A为酸,C和D为盐和水,该反应一定是中和反应 | |
| C. | 若B是氧化铜、D为铜,该反应可能是置换反应 | |
| D. | 若8gA与12gB恰好完全反应,则生成的C、D的质量和为20g |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com