
【题目】我国化工专家侯德榜的“侯氏制碱法”为世界制碱工业作出了突出的贡献。他以食盐、水、氨气、二氧化碳为原料,先制得碳酸氢钠和氯化铵,进而生产出纯碱。表格中是几种物质在不同温度时的溶解度:
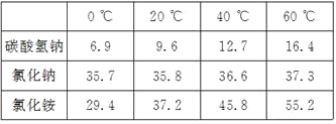
(1)从表中数据可以看出,温度对_____的溶解度影响不大。
(2)要使氯化铵饱和溶液中的氯化铵结晶析出,在____(填“较高”或“较低”)温度下进行比较合适。
(3)写出“侯氏制碱法”制碳酸氢钠的方程式_____。
(4)有人认为侯氏制碱法的优点有四:
A 生产过程中部分产品可选为起始原料使用
B 副产品是一种可利用的氮肥
C 反应不需要加热
D副产物不会造成污染环境
你认为其中正确的是___。
【答案】氯化钠 较低 NH3+H2O+CO2+NaCl===NaHCO3↓+NH4Cl ABD
【解析】
(1)从表中可以看出,温度对NaHCO3和NH4Cl的溶解度的影响都比较大,而对NaCl的溶解度影响不大,故选氯化钠。
(2)随着温度的升高,NH4Cl的溶解度变大,且受温度变化影响大,故可以通过在较高温度下配制NH4Cl的饱和溶液,然后再降温,结晶析出NH4Cl的办法将NH4Cl从溶液中分离出来。(3)侯氏制碱的原理:先将氨气通入饱和食盐水中而成氨盐水,再通入二氧化碳生成溶解度较小的碳酸氢钠沉淀和氯化铵溶液,故化学方程式:NaCl+NH3+H2O+CO2===NaHCO3↓+NH4Cl。
(4)根据氨碱法制纯碱的实验原理进行分析,以食盐(氯化钠)、石灰石(经煅烧生成生石灰和二氧化碳)、氨气为原料来制取纯碱。先使氨气通入饱和食盐水中而成氨盐水,再通入二氧化碳生成溶解度较小的碳酸氢钠沉淀和氯化铵溶液,即NaCl+NH3+H2O+CO2===NaHCO3↓+NH4Cl。将经过滤、洗涤得到的NaHCO3微小晶体,再加热煅烧制得纯碱产品。A项,烧制时放出的二氧化碳气体可回收循环使用,含有氯化铵的滤液与石灰乳混合加热,所放出的氨气可回收循环使用,正确;B项,副产品是氯化铵,其中含有氮元素,是一种氮肥,正确;C项,碳酸氢钠分解制纯碱时需要加热,错误;D项,氯化铵是一种氮肥,可再利用,不是污染物,正确。故选ABD。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
【题目】某化学兴趣小组的同学学习“灭火器原理”后,设计了如下图所示实验,并对反应后瓶中残留废液进行探究。
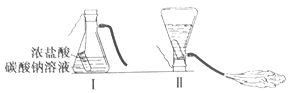
(提出问题)废液中所含溶质是什么?
(猜想与假设)
猜想1:废液中的溶质是NaCl、Na2CO3和HCl
猜想2:废液中的溶质只有NaCl
猜想3:废液中的溶质是NaCl、HCl
猜想4:废液中的溶质是______。
(讨论与交流)
小明认为猜想I无需验证就知道是错误的,他的理由是_____(请用化学方程式说明)。
(实验与结论)
(1)小亮同学为验证猜想3,取少量废液装入试管中,然后滴入酚酞溶液,发现溶液不变色,于是小亮认为猜想3正确。你认为他的结论____(填“正确”或“错误”),理由是______________。
请你另设计实验方案验证猜想3:
实验步骤 | 实验现象 | 实验结论 |
__________________ | __________________ | 猜想3正确 |
(2)验证猜想4,可选择的试剂有____________。
A.酚酞溶液B.氢氧化钾溶液C.稀硫酸D.氯化钡溶液
(拓展与应用)若废液中的溶质是NaCl和HCl,根据盐酸的性质,无需另加试剂,只要对废液进行____操作,即可从废液中得到NaCl固体。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用铝土矿(主要含SiO2、Al2O3和少量Fe2O3等)制取铝硅合金材料有干法、湿法等方法,其中干法制备的工艺流程如图所示。
(已知:I.SiO2不溶于水、不与硫酸反应。Ⅱ.转化率是反应物转化为生成物的百分率。)
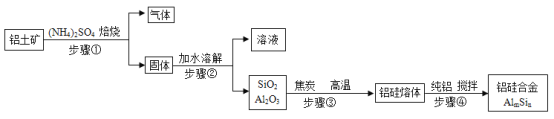
(1)铝硅合金的硬度比纯铝的硬度_______。
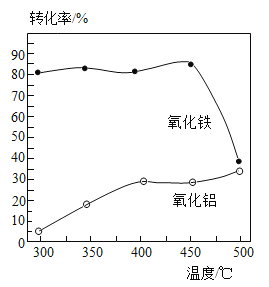
(2)步骤①中焙烧除铁的反应为:4(NH4)2SO4+Fe2O3![]() 2NH4Fe(SO4)2+3H2O+6NH3↑(Al2O3部分发生类似反应,SiO2不发生类似反应)。已知Fe2O3、Al2O3转化为硫酸盐的转化率与温度的关系如图所示,则焙烧除铁最适宜的温度为_______℃。
2NH4Fe(SO4)2+3H2O+6NH3↑(Al2O3部分发生类似反应,SiO2不发生类似反应)。已知Fe2O3、Al2O3转化为硫酸盐的转化率与温度的关系如图所示,则焙烧除铁最适宜的温度为_______℃。
(3)步骤②中包括加水溶解、_______、洗涤等操作。
(4)步骤③中利用焦炭还原SiO2、Al2O3会产生中间体SiC、Al4C3.写出高温下Al4C3与Al2O3反应生成A1和CO的化学方程式:_______。
(5)若用湿法处理铝土矿,加过量的硫酸浸取,所得溶液中的阳离子有_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小明对铁的锈蚀进行如下探究,室温时,将包有样品的滤纸包用大头针固定在橡胶塞上,迅速塞紧,装置如图,观察到量筒内水沿导管慢慢进入广口瓶(净容积为146 mL)。当温度恢复至室温,且量筒内水面高度不变时读数(此时瓶内氧气含量近似为零)。记录起始和最终量筒的读数以及所需时间如表
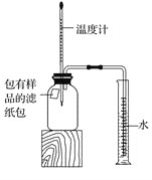
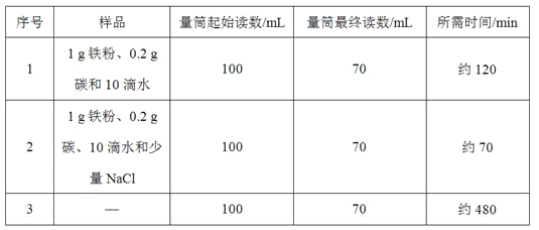
(1)实验①和②说明NaCl可以____铁锈蚀的速率。
(2)实验开始后,广口瓶内温度有所上升,说明铁的锈蚀过程是____(填“放热”或“吸热”)过程。
(3)实验结束后取出滤纸包,观察到有红棕色物质生成,该物质的化学式是______。
(4)已知碳能够加快铁的生锈速度,小明想通过实验①和③是探究碳对铁锈蚀速率的影响,请在表格空白处填写实验③的样品组成___。
(5)该装置还可用于测量空气中氧气的含量,根据上述数据计算氧气的体积含量是___(小数点后保留1位)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】生活中处处有化学,小明把学到的化学知识用于生活中,进行下列探究.

(1)如图所示,小明把一只新鲜鸡蛋放入盛水的玻璃杯中,鸡蛋沉入水底(蛋壳的主要成分是碳酸钙).若向玻璃杯中逐渐滴加浓盐酸,鸡蛋壳表面将出现的现象是_____,相应的化学反应方程式为_____.
(2)小明同学在家里做了如右图所示的小实验.
①图Ⅰ中观察到的主要现象是鸡蛋壳表面有气泡产生,蜡烛火焰熄灭.由此得出有关CO2性质的结论是_____.并依此性质确定CO2的一个主要用途是_____.
②当蜡烛熄灭后,在玻璃杯口迅速盖﹣块蘸有石灰水的玻璃片(见图Ⅱ).观察到的现象是玻璃片上的石灰水_____,此现象说明在杯中有_____气体产生,写出气体与石灰水反应的化学方程式_____.
(3)小明把含碳酸钙85%的鸡蛋壳20g和足量的稀盐酸反应,计算产生的气体是多少克?_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】Na2CO3、CaCO3、KHCO3、MgCO3分别和盐酸反应,下列分析不正确的是( )
A. 当Na2CO3和CaCO3的质量相等,盐酸足量时,CaCO3生成的CO2气体质量较多
B. 当CaCO3、KHCO3、MgCO3足量,盐酸等质量等浓度时,生成CO2气体的质量相等
C. 当CaCO3和KHCO3的质量相等,盐酸足量时,生成CO2气体的质量相等
D. 当Na2CO3、CaCO3、MgCO3足量,盐酸等质量等浓度时,生成CO2气体的质量相等
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】以软锰矿粉(主要含MnO2,还有少量Fe2O3)为原料制取MnCO3的流程如图1.
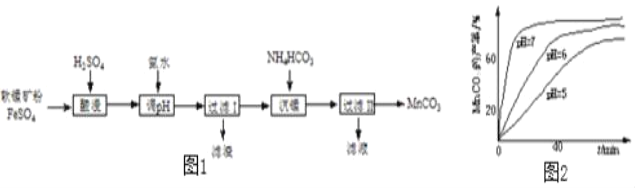
(1)“酸浸”时发生的反应有2FeSO4+MnO2+2H2SO4=_____+MnSO4+2H2O和_____。
(2)“过滤Ⅰ”所得滤渣的主要成分是_____。
(3)“沉锰”时测得MnCO3的产率与溶液pH、反应时间t的关系如图2,反应要控制pH=_____,其理由是_____、_____。
(4)“过滤Ⅱ”所得滤液中溶质的主要成分是_____。
(5)为测定某软锰矿中MnO2的质量分数,称取2.0 g软锰矿样品,加入3.35 g草酸钠(Na2C2O4)固体,再加足量稀硫酸(杂质不参加反应),充分反应后,过量的Na2C2O4用31.6 g/L KMnO4溶液进行反应,当滴入10.0 mL KMnO4溶液时恰好完全反应。
已知:①MnO2+Na2C2O4+2H2SO4=MnSO4 +2CO2↑+2H2O+Na2SO4 ;②2KMnO4+5Na2C2O4+8H2SO4=2MnSO4+5Na2SO4+K2SO4+10CO2↑+8H2O.
求该软锰矿中MnO2的质量分数。_____(相对分子质量:KMnO4 158;Na2C2O4 134;MnO2 87)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】1kg不同燃料燃烧产生CO2和SO2的质量如表所示。
燃料 | 燃烧产物质量/g | |
CO2 | SO2 | |
汽油 | 2900 | 5.0 |
天然气 | 2500 | 0.1 |
煤 | 2500 | 11.0 |
①其中较清洁的燃料是______,使用______做燃料时最易形成酸雨。
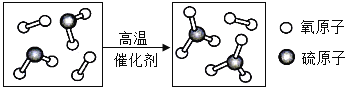
②酸雨形成过程中某一步反应的微观示意图如下图所示。则该反应的化学方程式为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com