
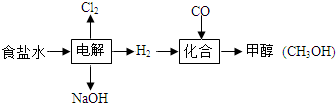
分析 (1)根据氯化钠溶液在通电的条件下生成氢氧化钠、氢气和氯气进行分析;
(2)根据元素质量守恒进行计算;
(3)根据化学方程式和题中的数据计算需要的氯化钠溶液质量.
解答 解:(1)氯化钠溶液在通电的条件下生成氢氧化钠、氢气和氯气,化学方程式为:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑,在实验室进行电解水的实验中,为了增强导电性,往往向水中加入少量稀硫酸,而不能加入氯化钠,理由是:电解食盐水得不到氧气,而是生成氯气;
(2)甲醇中的氢元素全部来自氢气,所以需要的氢气质量为:80t×$\frac{4}{32}$×100%=10t;
(3)设生产10吨氢气需要氯化钠的质量为x
2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+Cl2↑+H2↑
117 2
x 10 t
$\frac{117}{x}$=$\frac{2}{10t}$
x=585 t
需要26%的食盐水的质量为:$\frac{585t}{26%}$=2250t.
答:该工厂每生产80吨甲醇需要消耗2250吨26%的氯化钠溶液.
(1)2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑,电解食盐水得不到氧气,而是生成氯气;
(2)10;
(3)2250t.
点评 本题主要考查了化学方程式的书写和化学方程式的计算,难度不大,注意解题的规范性.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:解答题
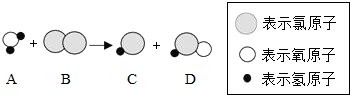 水是宝贵的自然资源,我们要认识它,爱护它.
水是宝贵的自然资源,我们要认识它,爱护它.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 红磷在空气中燃烧产生大量白色烟雾 | |
| B. | 木炭在空气中剧烈燃烧,发出白光 | |
| C. | 氢氧化钠溶液滴入硫酸铜溶液中,产生蓝色絮状沉淀 | |
| D. | 碱式碳酸铜粉末与稀盐酸反应,产生大量气泡,绿色溶液变成蓝色 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
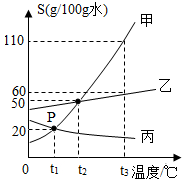 如图是甲、乙、丙三种固体物质的溶解度曲线.
如图是甲、乙、丙三种固体物质的溶解度曲线.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com