
【题目】已知:Mg(OH)2 = MgO+H2O。一定质量的Mg(OH)2和MgO的混合物加热一段时间后,将生成的气体通入到浓硫酸中,增重1.8g,已知剩余固体的质量为13.8g,剩余固体中Mg元素的质量为7.2g,下列说法错误的是
A. 剩余固体为混合物
B. 原混合物中Mg元素的质量为7.2g
C. 混合物中Mg(OH)2与MgO的质量之比为29∶20
D. 加热前后的固体分别与相同浓度稀盐酸恰好完全反应所消耗盐酸质量相等
【答案】C
【解析】氧化镁中镁元素质量分数是![]() ×100%=60%。A、反应后剩余固体中镁元素质量分数是
×100%=60%。A、反应后剩余固体中镁元素质量分数是![]() ×100%=52.17%,剩余固体为混合物,故A正确;B、根据质量守恒定律知,原混合物中Mg元素的质量是7.2g,故B正确;C、Mg(OH)2→H2O,混合物中Mg(OH)2 质量应是5.8g,反应生成的氧化镁应是4g,混合物中Mg(OH)2与MgO的质量之比为5.8g∶﹙13.8g -4.0g﹚=29∶49,故C错误;D、根据质量守恒定律知,加热前后的固体分别与相同浓度稀盐酸恰好完全反应所消耗盐酸质量相等,故D正确。
×100%=52.17%,剩余固体为混合物,故A正确;B、根据质量守恒定律知,原混合物中Mg元素的质量是7.2g,故B正确;C、Mg(OH)2→H2O,混合物中Mg(OH)2 质量应是5.8g,反应生成的氧化镁应是4g,混合物中Mg(OH)2与MgO的质量之比为5.8g∶﹙13.8g -4.0g﹚=29∶49,故C错误;D、根据质量守恒定律知,加热前后的固体分别与相同浓度稀盐酸恰好完全反应所消耗盐酸质量相等,故D正确。
点睛∶任何一个化学反应都必然遵循质量守恒定律,根据化学方程式可以计算反应物和生成物的质量。


科目:初中化学 来源: 题型:
【题目】通过对化学的学习,同学们已掌握了实验室制取气体的有关规律,另设计了几套实验装置进行研究,请结合下图1回答问题:

(1)写出标有数字的仪器名称:①________
(2)同学们想用高锰酸钾制取一瓶较纯净的氧气,他应选择上述装置中的A和____(填A-F序号)进行组装,而小明认为A装置中还缺少_______;该反应的化学方程式为_____________。
(3)实验室制取氢气若用 C 装置,在有孔塑料板上放置的药品是_____,该装置的优点是_______;
(4)①如图2是同学们设计的甲、乙、丙一组“吹气球”的实验,请回答:
甲装置中,向a中加入一定量水后会看到_____________,一段时间内观察到气球大小不变化,说明该装置气密性良好。气密性良好的乙装置中,若锥形瓶中装有NaOH固体,向锥形瓶加入分液漏斗中的水,则气球胀大的主要原因是________________。气密性良好的丙装置中,若锥形瓶中盛满CO2,欲使气球胀大,加入分液漏斗中的液体最好是_______。
A.稀硫酸溶液 B.NaOH溶液 C.NaCl溶液 D. NH4NO3溶液
②如图3装置丁是同学们利用医用输液观察滴液快慢的滴壶,用它作微型洗气装置,请回答:气体应从_________(填“b”或“c”)进入。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氯化钠在自然界中分布很广,海水里含大量氯化钠.某氯化钠粗品中含少量氯化镁和氯化钙,某化学兴趣小组设计提纯方案如下:
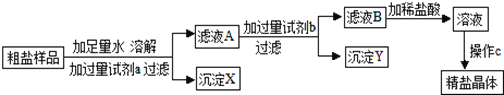
(1)方案中加入过量试剂a若为氢氧化钠溶液,则其目的是为了除去氯化钠粗品中的某种杂质,写出该反应的化学方程式 ;
(2)在过滤操作中,除用到带铁圈的铁架台、烧杯、玻璃棒外,还需要用到玻璃仪器是 ;
(3)方案中加入过量试剂b应为 溶液;
(4)向滤液B滴加稀盐酸的过程中,当观察到溶液的现象为 时,应停止滴加,写出相关的化学方程式 。
(5)操作C的名称为 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】通过一年的化学学习,你已经掌握了一些实验室制取气体的相关规律,以下是老师提供给大家的一些装置,请你回答下列问题:
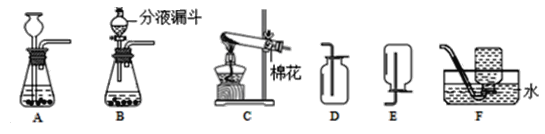
(1)实验室用二氧化锰和过氧化氢溶液制取氧气的化学方程式是________________,若要较好地控制产生氧气的速度,应选用的发生装置是__________(填字母编号)。
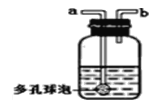
(2)实验室用大理石与稀盐酸制备CO2的化学方程式为_____________, 收集装置最好选择_______(填字母编号)。为了收集干燥的二氧化碳气体,可把气体通过下图的装置中进行干燥再收集。则下图瓶中的溶液是____________(写名称),装置中的多孔球泡的作用是____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】一定条件下,4.8 g CH4与12.8 g O2恰好完全反应,生成10.8 g H2O、5.6 g CO和物质X。则X的质量为______g;该化学方程式为________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】钙及其化合物在生产、生活中具有广泛的应用
(一)钙及其化合物的应用
(1)青少年缺“钙”易患的疾病是________。
(2)混凝土中也含有一定量的含钙物质,钢筋与混凝土混合形成钢筋混凝土,以上叙述中不涉及的材料是_________。 a.无机材料 b.合成材料 c.复合材料
(3)即热型快餐加热原理是利用生石灰和水反应放热,用方程式表示其反应__________。
(二)过氧化钙(CaO2)的性质
(1)CaO2中氧元素的化合价为_____________。
(2)CaO2能与稀盐酸发生复分解反应,反应的化学方程式为_____________。
(3)鱼类长途运输的增氧剂的主要成分为CaO2,它与水缓慢反应生成O2,还生成一种碱,其化学式为_______,Na2O2也能与水反应,原理与CaO2相同,但却不能作为鱼虾运输的供氧剂,请分析可能的原因___________________。
(三)过氧化钙晶体的制备
(资料)过氧化钙晶体(CaO2·yH2O),常温为白色,能溶于酸,难溶于酒精。
制备原理:CaCl2+H2O2+NH3+H2O ![]() CaO2·yH2O↓+NH4Cl,装置如下。
CaO2·yH2O↓+NH4Cl,装置如下。
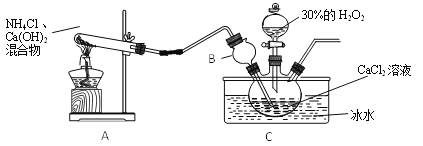
(1)装置A中试管内发生反应的化学方程式为______________________。
(2)装置C采用冰水浴控制温度在0℃左右,可能的原因主要有:
Ⅰ. 该反应是放热反应,温度低有利于提高CaO2·yH2O产率;
Ⅱ. _____________________________。
(3)反应结束后,经过滤、洗涤、低温烘干可获得CaO2·yH2O。
①洗涤时采用95%的酒精溶液洗涤的优点是_________________。
②检验晶体已洗涤干净的方法为________________________。
(四)过氧化钙晶体组成的测定
称取21.6克晶体用热分析仪对其进行热分解实验,并绘制成固体质量与温度关系图(过氧化钙晶体受热时会先失去结晶水)
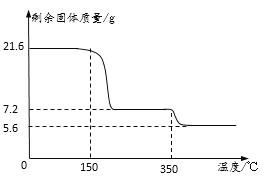
(1)0—150℃质量不发生改变的原因是______________________。
(2)根据上图可知y=________。
(3)350℃时发生反应的化学方程式为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用质量相等的锌粉和铁粉,分别与溶质质量分数相同且等质量的稀盐酸充分发生反应,产生氢气的质量与时间的关系如图所示。

请回答下列问题:
(1)表示锌粉与稀盐酸反应的曲线为 (填a或b)。
(2)对于a曲线表示的反应,物质 (填名称)有剩余。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】生物体中含有多种氨基酸(结构如图所示)。下列有关叙述正确的( )
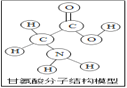
A. 甘氨酸是有机高分子化合物
B. 一个甘氨酸分子中含有10个原子
C. 甘氨酸是由碳、氢、氧、氮四种原子构成的
D. 甘氨酸中碳元素与氧元素的质量比为1:1
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是甲、乙、丙三种物质的溶解度曲线,下列说法不正确的是
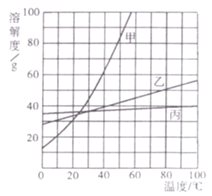
A. 甲的溶解度受温度影响最大
B. 10℃时,三种物质的溶解度大小顺序为丙>乙>甲
C. 30℃时,乙、丙两种物质的饱和溶液溶质质量分数相等
D. 50℃时,分别将40g甲、乙两种物质放入100g水中,均得到饱和溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com