
| A. | X为H2O | |
| B. | 该反应中MnO2为催化剂 | |
| C. | 该反应中共有3种氧化物 | |
| D. | 反应前后锌元素的化合价发生了变化 |
分析 A、根据化学反应方程式Zn+2MnO2+X═ZnO+2MnOOH.利用质量守恒定律中的守恒法来解答X的化学式;
B、根据反应过程来分析;
C、根据氧化物的概念分析;
D、单质的化合价为0.
解答 解:A、由化学反应方程式为Zn+2MnO2+X═ZnO+2MnOOH.Zn、Mn元素的原子的个数反应前后相等,
根据质量守恒定律可知,H、O元素的原子个数前后也应相等,
反应后共有2个H原子,5个O原子,而反应前共有4个O原子,
则X中共有2个H原子,1个O原子,
则X的化学式为H2O,
B、催化剂能改变化学反应的速率,而本身的质量和化学性质不变.而在该反应中二氧化锰是反应物,质量减少,故错误;
C、氧化物是由两种元素组成,其中一种是氧元素的化合物,MnO2、H2O、ZnO是氧化物,故正确;
D、反应前后锌元素以单质的形式存在,化合价为0,反应后锌元素以化合物的形式存在,化合价不为0,故正确;
故选B.
点评 本题属于信息给予题,解题的关键是认真阅读题干,提取有用的信息,分析、判断有关的问题.


科目:初中化学 来源: 题型:实验探究题
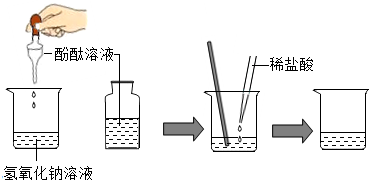
| 实验操作 | 实验现象 | 实验结论 |
| 取少量反应后的溶液于试管中滴入Na2CO3溶液 | 有气泡产生 | 猜想二成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
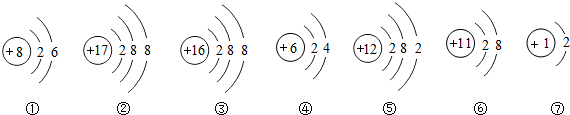
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 实验目的 | 实验操作 |
| A | 检验某气体是否为CO2 | 将燃着的木条伸入气体中 |
| B | 鉴别NaCl溶液和稀盐酸 | 滴加无色酚酞溶液 |
| C | 除去CaCO3中的Na2CO3 | 加水溶解,过滤 |
| D | 除去CO2中的CO | 点燃 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 工厂排放的废水:pH=4.3 | B. | 温瑞塘河水:pH=6.5 | ||
| C. | 瓯江水:pH=7.0 | D. | 楠溪江江水:pH=7.3 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
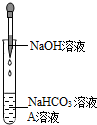 同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?在老师的帮助下,他们通过以下探究过程证明NaHCO3溶液与NaOH溶液发生了反应.
同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?在老师的帮助下,他们通过以下探究过程证明NaHCO3溶液与NaOH溶液发生了反应.| NaHCO3溶液 | NaOH溶液 | Na2CO3溶液 | |
| 加入稀盐酸 | 产生气泡 | Ⅰ | 产生气泡 |
| 加入澄清石灰水 | 溶液变浑浊 | 无明显变化 | Ⅱ |
| 加入CaCl2溶液 | 无明显变化 | 溶液变浑浊 | 溶液变浑浊 |
| 加热溶液至沸腾,将 气体通入澄清石灰水 | 澄清石灰水 变浑浊 | 澄清石灰水 无明显变化 | 澄清石灰水 无明显变化 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 291 | B. | 174 | C. | 117 | D. | 57 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com