
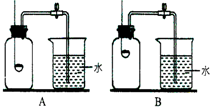
 某校化学兴趣小组就空气中氧气的含量进行了如下实验探究
某校化学兴趣小组就空气中氧气的含量进行了如下实验探究| 组别 | 1 | 2 | 3 | 4 | 5 | 6 |
| 进入集气瓶中水的体积/mL | 20 | 21 | 19 | 20 | 22 | 19 |
分析 (1)蜡烛、硫和木炭与氧气反应,生成物中有气体,不能准确测定空气中氧气的含量,只有红磷在空气中与氧气反应生成固体物质,不影响空气成分的测定,据此分析判断;
(2)为保证红磷与空气中的氧气充分反应,必须把红磷放在集气瓶的中下部;在测定空气中氧气的含量时,由于氧气参加了反应,瓶内压强减小,应检查装置的气密性;
(3)通过实验数据分析空气中氧气的体积分数,根据实验的现象分析剩余气体的性质.
解答 解:(1)蜡烛、硫和木炭与氧气反应,生成物中有气体,不能准确测定空气中氧气的含量,红磷不会跟空气中的其他成分反应,而且生成物为五氧化二磷固体;所以在测定空气中氧气的含量是应选用红磷;只有红磷足量或过量,才能完全消耗集气瓶中的氧气;
(2)为保证红磷与空气中的氧气充分反应,必须把红磷放在集气瓶的中下部;两套装置,合理的是A装置;为了确保实验的成功,在装药品之前应该检查装置的气密性.
(3)根据6组数据的平均值是20mL,说明氧气约占空气体积的五分之一;通过实验还可以推断集气瓶中剩余气体的性质是难溶于水,不能燃烧,不支持燃烧等.
故答为:(1)B;足量;(2)A;检查装置的气密性;(3)$\frac{1}{5}$;难溶于水;不能燃烧;不支持燃烧.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.


 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
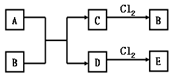 绝大多数金属都能与Cl2直接化合生成金属氯化物,如2Na+Cl2点燃═2NaCl,Cu+Cl2点燃═CuCl2等.已知A、B、C、D、E五种物质有如图转化关系(个别反应条件已略去).已知A是地壳中含量仅次于铝的金属元素的单质,C为紫红色金属单质,A、C都能与Cl2直接化合生成相应的金属氯化物B、E.回答下列问题:
绝大多数金属都能与Cl2直接化合生成金属氯化物,如2Na+Cl2点燃═2NaCl,Cu+Cl2点燃═CuCl2等.已知A、B、C、D、E五种物质有如图转化关系(个别反应条件已略去).已知A是地壳中含量仅次于铝的金属元素的单质,C为紫红色金属单质,A、C都能与Cl2直接化合生成相应的金属氯化物B、E.回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 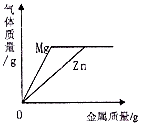 向两份完全相同的稀H2SO4中分别加入足量的锌粉、镁粉 | |
| B. | 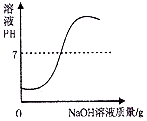 向一定量的稀盐酸中加入过量的NaOH溶液 | |
| C. | 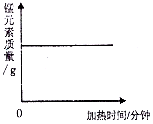 加热一定质量的KMnO4固体 | |
| D. | 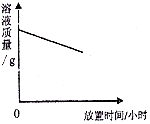 将一定量的浓H2SO4敞口放置在空气中 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验步骤 | 设计要求 |
| ①准备两个大小相同的烧杯,分别标为A、B;向两烧杯中分别倒入30克粗细相同的食盐. | 选择合适的实验器材 |
| ②向A烧杯倒入20克水,向B烧杯倒入60克水. | 设置对照实验 |
| ③都用玻璃棒充分搅拌直到A、B两烧杯底部的食盐不再溶解为止,过滤、干燥剩余食盐 | 控制实验条件 |
| ④称量并记录,并进行统计分析. | 观察和记录 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
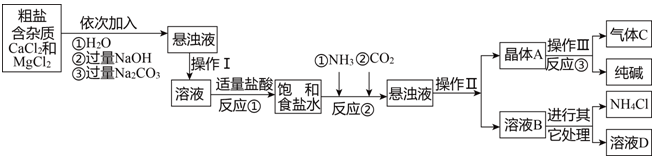
| 物质 | NaCl | NaHCO3 | NH4Cl | NH3 | CO2 |
| 溶解度 | 36.0g | 9.6g | 37.2g | 710g | 0.9g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
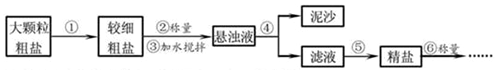
| 温度/℃ | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | 氯化钠 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| 硝酸钾 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com