
| A. |  氢气的验纯 | B. | 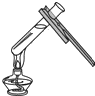 给盛有液体的试管加热 | ||
| C. | 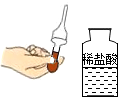 滴管取液后移动 | D. | 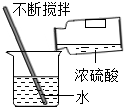 稀释浓硫酸 |
分析 A、根据检验氢气纯度的方法,进行分析判断.
B、根据给试管中的液体加热的方法进行分析判断.
C、根据滴瓶上的滴管的使用方法进行分析判断.
D、根据浓硫酸的稀释方法(酸入水,沿器壁,慢慢倒,不断搅)进行分析判断.
解答 解:A、检验氢气纯度的方法:用排水法收集一试管氢气,用拇指堵住试管口,管口向下移近酒精灯火焰,松开拇指点火,如果听到尖锐的爆鸣声,表明氢气不纯,需要再收集,再检验,直到听到很小的响声,才表明氢气已经纯净,图中所示装置正确.
B、给试管中的液体加热时,用酒精灯的外焰加热试管里的液体,且液体体积不能超过试管容积的$\frac{1}{3}$,图中液体超过试管容积的$\frac{1}{3}$,图中所示操作错误.
C、为防止污染胶头滴管;使用滴管的过程中不可平放或倒置滴管,以防止污染胶头,故选项说法错误.
D、稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时地扩散;一定不能把水注入浓硫酸中;图中所示操作错误.
故选:A.
点评 本题难度不大,熟悉各种仪器的用途及使用注意事项、常见化学实验基本操作的注意事项是解答此类试题的关键.


科目:初中化学 来源: 题型:填空题
 A、B、C三种固体物质的溶解度曲线如图所示.
A、B、C三种固体物质的溶解度曲线如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A | B | C | D | |
| 需区分的物质 | 黄铜和黄金 | 聚乙烯(PE)和聚氯乙烯(PVC) | 锦纶布料和羊毛布料 | NH4NO3和NaOH固体 |
| 第一方案 | 分别取样,观察颜色 | 分别取样,观察颜色 | 分别取样,用手触摸 | 分别取样,加水充分溶解,加氯化铵溶液,加热,观察现象 |
| 第二方案 | 分别取样,在石棉网上高温灼烧,观察现象 | 分别取样,分别点燃,闻燃烧时产生的气味 | 分别取样,点燃,闻气味 | 分别取样,加水,滴加无色酚酞溶液,观察现象 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
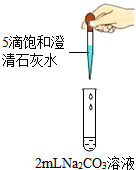 学习酸碱盐知识后,同学们知道碳酸钠溶液与氢氧化钙溶液能发生反应,可观察到溶液变浑浊.甲组同学进行如图1所示的实验,却未观察到预期现象.
学习酸碱盐知识后,同学们知道碳酸钠溶液与氢氧化钙溶液能发生反应,可观察到溶液变浑浊.甲组同学进行如图1所示的实验,却未观察到预期现象.| 实验目的 | 实验操作 | 实验现象 | |
| 探究猜想② | 取4支试管,向其中分别加入… | 碳酸钠溶液浓度/% | 是否浑浊 |
| 10 | 不浑浊 | ||
| 5 | 不浑浊 | ||
| 1 | 浑浊 | ||
| 0.5 | 浑浊 | ||

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com