
分析 根据在金属活动性顺序中,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来;在硝酸亚铁、硝酸银、硝酸钾的混合溶液中,加入一定质量的锌粉,锌比铁、银活泼,会置换出铁和银,铁会先于硝酸银反应,再与硝酸亚铁反应,锌会不会与硝酸钾反应等知识进行分析.
解答 解:在金属活动性顺序中,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来;在硝酸亚铁、硝酸银、硝酸钾的混合溶液中,加入一定质量的锌粉,锌比铁、银活泼,会置换出铁和银,铁会先于硝酸银反应,再与硝酸亚铁反应,锌会不会与硝酸钾反应,所以滤液中一定含有的溶质的化学式为KNO3、Zn(NO3)2,锌首先与硝酸银反应,所以滤渣中一定含有银,锌的质量较少时,还不会与硝酸亚铁反应,锌足量时,锌会有剩余,会置换出铁,所以滤渣中可能含有的物质的化学式为Fe、Zn.
故答案为:KNO3、Zn(NO3)2,Fe、Zn.
点评 本题难度不是很大,考查了金属活动性顺序的应用,掌握金属活动性顺序并能灵活运用是正确解答此类题的关键所在.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
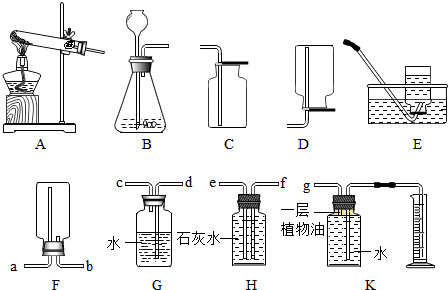
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验现象 |
| A | 除去CaO中混有的CaCO3 | 先加足量水,然后过滤 |
| B | 除去KCl中的少量CuCl2 | 先加入NaOH溶液至不再产生沉淀,再过滤 |
| C | 鉴别棉绒和羊毛绒 | 点燃,闻产生的气味,观察生成的灰烬 |
| D | 鉴别稀盐酸和氯化钠溶液 | 滴加酚酞试液,观察溶液颜色变化 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
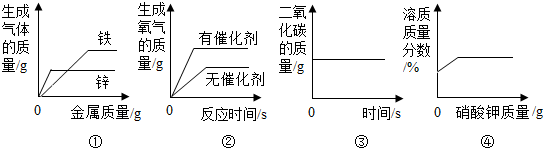
| A. | ①② | B. | ③④ | C. | ①②③ | D. | ①③④ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 滤渣中一定含Cu,可能含Zn | B. | 滤液中只有ZnSO4 | ||
| C. | 滤液中只有CuSO4 | D. | 向滤渣中滴加稀盐酸,无气泡产生 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 滤渣中只有Ag | B. | 滤渣中一定有Fe | ||
| C. | 滤渣中一定有Zn | D. | 滤渣中一定有Zn、Fe、Ag |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 养成“周密设计、规范操作”的良好实验习惯,是完成化学实验的关键.在化学课上,同学们对蓝色沉淀Cu(OH)2产生了浓厚的兴趣.
养成“周密设计、规范操作”的良好实验习惯,是完成化学实验的关键.在化学课上,同学们对蓝色沉淀Cu(OH)2产生了浓厚的兴趣.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com