
【题目】实验室可用下图装置模拟工业炼铁。
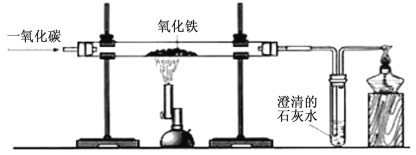
(1)一氧化碳与氧化铁(Fe2O3)反应的化学方程式是 ________________ 。
(2)实验前先通入 CO 的目的是_____________,反应后玻璃管中出现的现象是_____________。
(3)装置图末端的导气管口放一盏燃着的酒精灯,这样做的目的是__________________。
【答案】Fe2O3+3CO![]() 2Fe+3CO2 排净玻璃管内的空气 红色粉末逐渐变成黑色 点燃未反应的一氧化碳,防止污染空气
2Fe+3CO2 排净玻璃管内的空气 红色粉末逐渐变成黑色 点燃未反应的一氧化碳,防止污染空气
【解析】
(1)一氧化碳与氧化铁(Fe2O3)在高温条件下反应生成铁和二氧化碳,化学方程式是 Fe2O3+3CO ![]() 2Fe+3CO2 ;
2Fe+3CO2 ;
(2)点燃或加热可燃性气体与空气的混合物易发生爆炸,实验前先通入 CO 的目的是排净玻璃管内的空气防止加热时发生爆炸,氧化铁是红色固体,铁粉是黑色固体,反应后玻璃管中出现的现象是红色粉末逐渐变成黑色;
(3)一氧化碳是有毒气体,是空气污染物,一氧化碳可以燃烧转化成无毒无污染的二氧化碳。装置图末端的导气管口放一盏燃着的酒精灯,这样做的目的是点燃未反应的一氧化碳,防止污染空气。


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
【题目】化学来源于生活,又服务于生活,请用所学化学知识回答下列问题。
(1)日常生活中,切菜刀采用的防锈措施是_________________。
(2)古人在野外生火时常“钻木取火”。“钻木取火”满足的燃烧的条件是____(填序号)。
A.提供可燃物 B.与氧气接触 C.达到燃烧所需的最低温度
(3)下图金属应用的实例,主要利用金属的导热性的是_______(填序号);

A电缆 B.电热壶 C.金属丝 D.金属乐器
(4)氢氟酸(HF)能刻画玻璃,其中有一个化学反应的化学方程式是:CaSiO3+6HF=X+SiF4↑+3H2O,则X的化学式为_______________;
(5)钛合金与人体具有很好的“相容性”,可以用来制造人造骨。由此得知钛合金具有的优良性能是_____________。(答一点即可)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】黄铜矿(主要成分CuFeS2)经初步处理后,所得溶液甲中的溶质为硫酸铁和硫酸铜(溶质之间不发生反应)。某同学通过废铁屑与溶液甲反应,制取补血剂原料绿矾(FeSO4·7H2O)并得到副产品铜。主要步骤如图所示:
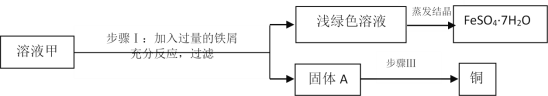
(1)已知步骤I中,铁与硫酸铁发生化合反应,请写出该反应的化学方程式_________。
(2)步骤Ⅰ中,生成铜的化学方程式_________。
(3)步骤Ⅰ中,加入的铁屑应过量的目的是_________。
(4)步骤Ⅲ得纯铜的方法是:加过量X、过滤、洗涤、干燥,其中X是_______(填名称)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学小组同学做镁条在空气中燃烧实验时,发现生成物中还有少量黑色固体,针对这一现象及相关问题,他们开展了如下探究,请仔细阅读并参与他们的探究之旅。
(探究目的)探究黑色固体是镁与空气中什么物质反应产生的?
(查阅资料)1.稀有气体一般与其他物质反应 2.光亮的镁条与水反应,表面会生成白色固体。
(分析猜想)分析空气中各种成分,进行猜想:
(1)猜想①是氧气 猜想②是氮气 猜想③是__________________
(实验一)镁带与氧气的反应
(一)甲同学探究了影响过氧化氢制取氧气速度的某种因素,进行了三次实验并记录各收集相同体积氧气所需要的时间如下表
实验 | 过氧化氢的浓度 | 过氧化氢溶液质量/g | 二氧化锰质量/g | 收集时间/s |
1 | 10% | 20 | 40 | |
2 | 15% | 20 | 1 | 20 |
3 | 20% | X | 1 | 12 |
(2)第 3 次实验中,X 的值应为_____
(3)实验结论:在相同条件下,___________________过氧化氢分解得越快。
(二)乙同学在量筒中盛满水,倒置于水槽中,通过分液漏斗把 20mL 某浓度的过氧化氢溶液加入锥形瓶中,记录量筒中气体的体积(如图 )。数据如下表:
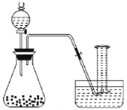
时间/min | 1 | 3 | 5 | 7 | 9 | 10 |
量筒读数/mL | 60.0 | 82.0 | 88 | 89.5 | 90 | 90 |
(4)请根据以上过程和实验数据综合分析,最终生成氧气的体积是_____mL
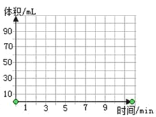
(5)请在下面坐标图中绘制出 0~10 min 生成氧气体积随时间变化的曲线_____________。
(三)燃烧镁带,观察现象
将镁带打磨光亮,点燃伸入盛满氧气的集气瓶中,产生大量白烟,生成白色固体。实验结论:镁与氧气反应生成白色的氧化镁
(实验二)镁带与氮气反应
(一)收集氮气
(二)燃烧镁带,观察现象
将镁带打磨光亮,点燃伸入盛满氮气的集气瓶中,瓶内壁附着一层淡黄色的固体。
(6)实验结论:镁与氮气在点燃条件下发生化合反应生成淡黄色的氮化镁(Mg3N2) 该反应的化学方程式是________
(探究结论 1)(7)综上分析,关于镁在空气中燃烧产生黑色固体的猜想是猜想__________(填序号)成立。
(探究结论 2)(8)如果用足量的镁代替红磷进行空气组成实验,实验测得氧气的体积分数比实际值______(填“偏大”或“偏小”)
(实验回顾)实验室常用红磷燃烧的方法测定空气中氧气含量(如图),由于红磷需要在瓶外点燃再伸入瓶内,常常带来污染以及误差。
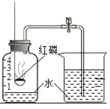
(实验改进)同学们选择了着火点更低的白磷,并对装置图做了改进(如图)。主要操作是:在实际容积为 180mL 的集气瓶里,先装进 50mL 的水,再按图连好仪器,按下热的玻璃棒,白磷立即被点燃。
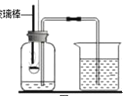
(9)白磷从燃烧到熄灭冷却的过程中,瓶内水面的变化是______________
(10)若实验中无误差,最终集气瓶中水的体积为__________________mL
(11)集气瓶里预先装置的 50mL 水的作用,其一是为了加快集气瓶的冷却速度,其二则主要是_____________
(实验与交流)
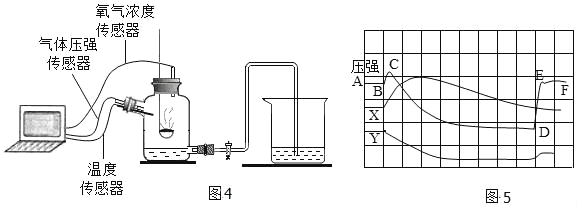
(12)为了帮助同学们更好地理解空气中氧气含量的实验原理,老师利用传感器技术定时测定了实验装置(图 4)内的压强、温度和氧气浓度,三条曲线变化趋势如图 5 所示。Y 曲线表示的是_______________(填“温度”或“氧气浓度”或“压强”)变化趋势;X 曲线中 CD 段上升的原因是___________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向盛有一定质量AgNO3和Cu(NO3)2的混合溶液中的烧杯中逐渐加入过量Zn粉,并边加边搅拌,溶液质量与加入Zn的质量关系如图所示.
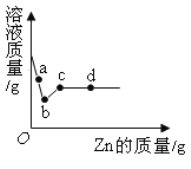
(1)写出![]() (不包括b点)段反应的化学方程式_______.
(不包括b点)段反应的化学方程式_______.
(2)分别写出a、d所对应溶质的化学式_______。
(3)指出a~ b段溶液质量变化的原因_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水在生活、生产和科学实验中非常重要,请回答下列问题。
(1)下列有关水的说法正确的是___________。
A.活性炭可以吸附水中的异味 B.生活中常用煮沸的方法软化硬水
C.生活污水可以任意排放 D.经处理后的工业用水可以循环使用
(2)用如图所示装置进行可燃物燃烧条件的探究实验,已知白磷的着火点为 40℃,红磷的着火点为 240℃(白磷、红磷均不超 过绿豆大小,锥形瓶中的白磷 A 与红磷被铜条隔开)。
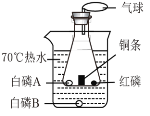
①写出锥形瓶中发生反应的化学方程式___________。
②能得到“可燃物燃烧需要氧气”这一结论的现象为___________。
③该实验中热水的作用___________。
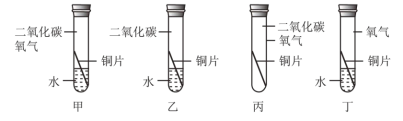
(3)根据铜锈蚀生成铜绿[Cu2(OH)2CO3],某同学猜想:铜锈蚀时要有氧气、水和二氧化碳 共同参与。为证明铜生锈“必须有水参与”,需要进行下图所示实验中的___________。
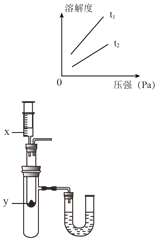
(4)不同温度下,二氧化碳在水中的溶解度随压强变化如右图所示。 图中 t1 对应的温度为 20℃,则 t2 对应的温度___________(填字母)。
A.大于 20℃ B.小于 20℃ C.无法确定
(5)按如图所示装置,将液体 x 注入装有固体 y 的试管中,会导致 U形管中右端液面升高,则可能的组合是___________。

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图为许多家庭使用的液化石油气,其主要成分是丙烷(C3H8)、丁烷、丙烯和丁烯等可燃性气体,它们燃烧时都能与氧气发生反应,放出大量的热量,充分燃烧时的生成物均为水和二氧化碳。

(1)保持丙烷气体化学性质的最小粒子是___________。
(2)丙烷中碳、氢元素的质量比为________。
(3)丙烷中碳、氢元素的原子个数比为__________。
(4)请写出丙烷气体充分燃烧的化学方程式:___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】乙酸(俗称醋酸)是我们生活中常见的一种饱和脂肪酸,下表列举了部分饱和脂肪酸的化学式、熔点和沸点,请你根据表中信息回答下列问题:
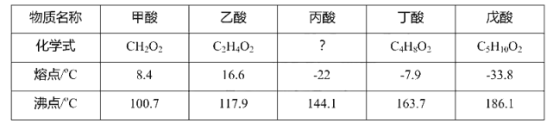
(1)试推测丙酸的化学式为__________;
(2)饱和脂肪酸的命名与分子中的______原子个数有关;
(3)这五种饱和脂肪酸中氢元素的质量分数最大的是________(填物质名称);
(4)乙酸的水溶液中会含有较多的氢离子,则![]() 个氢离子可以表示为_______(填化学符号);
个氢离子可以表示为_______(填化学符号);
(5)甲酸与浓硫酸共热,常用于实验室制取一氧化碳,其化学方程式可以表示为: HCOOH![]() H2O+CO该反应所属的基本反应类型是___________.
H2O+CO该反应所属的基本反应类型是___________.
(6)下列有关戊酸的说法正确的是_______(填序号)
A.戊酸是由原子构成的 B.戊酸中含有氧分子
C.戊酸属于氧化物 D.戊酸分子中碳、氢、氧原子的个数比为5:10:2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】青龙山农场学校篮球挑战赛中运动员穿的篮球鞋在生产中所用的胶水含有正己烷(C6H14),请回答下列问题:
(1)正己烷是一种_______________(填“有机物”或“无机物”)
(2)正己烷的相对分子质量是________
(3)正己烷中氢、碳元素的质量比为________
(4)17.2g正己烷中碳元素的质量为________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com