
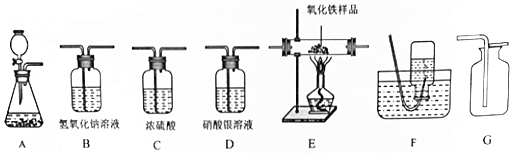
| 装置编号 | D | C1 | C2 | B |
| 试剂 | 硝酸银溶液 | 浓硫酸 | 浓硫酸 | 氢氧化钠溶液 |
| 现象或质量变化 | 无明显现象 | 增重1.0g | 增重2.7g | 增重0.66g |
分析 (1)①干燥氧气应该选择浓硫酸,然后用向上排空气法收集,可以据此解答该题;
②根据氧化氢以二氧化锰作催化剂分解为水和氧气写出该反应的化学方程式;
③根据使用分液漏斗的装置检查气密性方法进行分析;
(2)①根据加热颗粒颜色变化分析;
②二氧化碳和氢氧化钠反应生成碳酸钠,据反应物、生成物及反应条件写出方程式;
③根据HCl能与硝酸银反应生成白色沉淀分析;
④根据反应物、生成物,结合化学方程式进行计算分析.
解答 解:(1)①制取氧气应该选择A装置,干燥氧气应该选择浓硫酸,然后用向上排空气法收集,故正确的顺序为:A→C→F;
②过氧化氢以二氧化锰作催化剂分解为水和氧气;化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
③使用分液漏斗的装置检查气密性方法:关闭阀门,将导管一端放入水中,用水捂住锥形瓶,一段时间后,若水中的导管口有气泡冒出,手松开,水会倒流进导管口一段距离,则说明气密性良好;
(2)①装置E中是氧化铁发生还原反应的实验装置,能观察到的明显现象是红色的氧化铁颗粒逐渐变成了黑色;
②装置B中发生的反应是二氧化碳与氢氧化钠的反应,二氧化碳与氢氧化钠反应生成碳酸钠和水,其反应的化学方程式为:CO2+2NaOH=Na2CO3+H2O;
③当混合气体通入D中硝酸银溶液时,装置D中没有看到明显现象,这就说明混合气体中没有HCl气体,因为HCl气体会与硝酸银反应生成氯化银沉淀,故由此可知,混合气体中一定不含HCl气体;
④在C2中浓硫酸增重2.7g,说明氢气在与氧化铁反应时生成了2.7g水,在B中氢氧化钠溶液增重0.66g,说明混合气体中还含有一氧化碳,并与氧化铁发生反应,反应生成的二氧化碳质量为0.66g,由此可根据化学方程式计算出在氧化还原反应中氧化铁的质量,设,在氢气还原氧化铁反应中氧化铁的质量Xg,则
3H2+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3H2O
160 54
X 2.7g
$\frac{160}{54}=\frac{X}{2.7g}$
X=8g
设,在一氧化碳还原氧化铁反应中氧化铁的质量为Zg,则
Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
160 132
Z 0.66g
$\frac{160}{132}=\frac{Z}{0.66g}$
Z=0.8g
由此参加反应的氧化铁的质量为:8g+0.8g=8.8g;则氧化铁样品中氧化铁的质量分数为:$\frac{8.8g}{10g}×100%$=88%;
故答案为:(1)①ACG;②2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;③关闭阀门,将导管一端放入水中,用水捂住锥形瓶,一段时间后,若水中的导管口有气泡冒出,手松开,水会倒流进导管口一段距离,则说明气密性良好;(2)①红色固体变黑;②CO2+2NaOH=Na2CO3+H2O;③氯化氢;④88%;
点评 熟记实验室制取氢气的反应原理、注意事项以及物质的检验和除杂的知识等,并能灵活应用质量守恒定律和相关知识进行解题,要求同学们在平时的学习中加强基础知识的储备,以便能够灵活应用.


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:初中化学 来源: 题型:推断题
 A~L均为初中化学常见物质,其中A是大理石主要成分,B是人体胃酸的一种主要成分,E是钠盐,它们之间有如右图所示的相互转换关系(图中部分生成物已略去)请回答下列问题:
A~L均为初中化学常见物质,其中A是大理石主要成分,B是人体胃酸的一种主要成分,E是钠盐,它们之间有如右图所示的相互转换关系(图中部分生成物已略去)请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
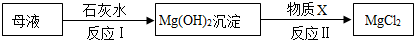
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验编号 药品 | 甲 | 乙 | 丙 | 丁 |
| 1g大理石 | 块状 | 块状 | 粉末状 | 粉末状 |
| 10g盐酸(过量) | 稀盐酸 | 浓盐酸 | 稀盐酸 | 浓盐酸 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
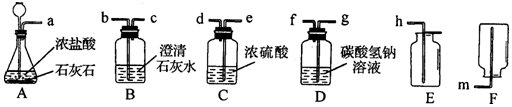
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 酸性 | 中性 | 碱性 | |
| 玫瑰花 | 粉红 | 粉红 | 绿 |
| 万寿菊花 | 黄 | 黄 | 黄 |
| 大红花 | 橙 | 粉红 | 绿 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com