
【题目】甲、乙、丙、丁四种物质在反应前后的质量关系如下图所示,下列有关说法错误的是
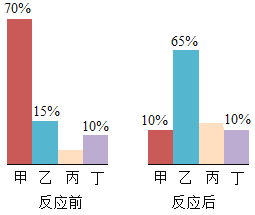
A. 反应前丙的质量分数为5%
B. 甲一定是化合物
C. 丁一定是催化剂
D. 该反应为分解反应
【答案】C
【解析】
由图中数据分析可知,反应前后甲的质量分数减少了70%-10%g=60%,故甲是反应物;同理可以确定乙是生成物,乙的质量分数增加了65%-15%g=50%;丁的质量不变,可能作该反应的催化剂,也可能没有参加反应。由质量守恒定律,反应后丙的质量应为1-10%-10%-65%=15%,质量分数增加,应为生成物。
A、反应前丙的质量分数为1-70%-15%-10%=5%,故选项说法正确;
B、该反应的反应物为甲,生成物是乙和丙,符合“一变多”的特征,属于分解反应,甲一定是化合物,故选项说法正确;
C、丁的质量不变,可能作该反应的催化剂,也可能没有参加反应,故选项说法错误;
D、反应的反应物为甲,生成物是乙和丙,符合“一变多”的特征,属于分解反应,故选项说法正确。
故选D。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
【题目】中国志愿者王跃参加了人类首次模拟火星载人航天飞行试验。有探测资料表明,火星上存在丰富的镁资源。在元素周期表中,镁元素的某些信息如图所示,下列说法不正确的是
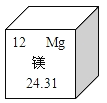
A. 镁元素属于非金属元素
B. 镁元素原子的核电荷数为12
C. 镁元素原子的核外电子数为12
D. 镁元素的相对原子质量为24.31
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】黑白复印机用的墨粉中常添加Fe3O4粉末,如图是氧化沉淀法生产复印用Fe304粉末的流程简图。(资料:+2价的铁元素容易被空气中的氧气氧化)
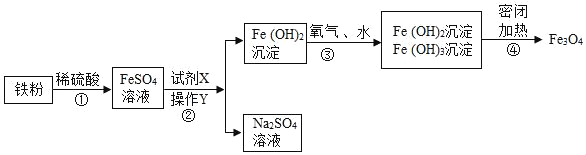
(1)判断铁粉己完全反应的现象是_____;
(2)操作Y的名称为_____,完成该操作所需的玻璃仪器有玻璃棒、烧杯、_____(填名称)。
(3)实验室在制备纯净的Fe(OH)2沉淀时,需要将吸有X试剂的胶头滴管伸到FeSO4溶液液面以下再滴,此操作的目的是_____。
(4)步骤②中涉及的反应方程式为_____,此反应的基本类型为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图的加热袋常用于野外加热食物。加热袋中的固体粉末含镁粉、铁粉和氯化钠,使用时向其中加入水袋中的水,即可产生大量热。实验小组针对放热过程中的反应原理展开探究。


【查阅资料】
常温下镁粉能与水发生置换反应,且放热。
【进行实验】
同学们用下图所示装置进行模拟实验:分别取不同成分的固体粉末放入甲中,通过分液漏斗向其中均加入8 mL水,读取甲中所得固液混合物的最高温度,实验记录如下表:
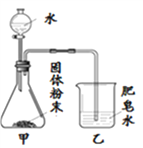
(实验时的室温为22.8℃)
实验序号 | A | B | C | D | E | F |
固体成分 | Mg | Fe | Mg+Fe | Mg+NaCl | Fe+NaCl | Mg+Fe+NaCl |
乙中现象 | 少量肥皂泡,难以点燃 | ______ | 少量肥皂泡,难以点燃 | 较多肥皂泡,点燃有爆鸣声 | 无肥皂泡 | 大量肥皂泡,点燃有爆鸣声 |
混合物温度 | 23.1℃ | 22.8℃ | 23.1℃ | 24.2℃ | 22.8℃ | 27.2℃ |
【解释与结论】
(1)实验B,乙中现象为_______________。
(2)实验A证明了镁粉与水能反应,完成该反应的化学方程式Mg+2H2O=____+H2 ![]() 。
。
(3)使镁粉与水迅速反应并放热的最佳方法是向镁粉中加入_____________。
【反思改进】
(4)同学们分析实验数据发现,升高的温度没有达到食品加热袋的效果,其可能的原因是___________。
(5)同学们根据实验结果进一步猜测,实验F中的反应结束后,甲中剩余固体混合物中仍然含有铁粉,检验其铁粉存在的的实验方案为:取少量固体混合物________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学反应常伴随着能量的变化,从能量角度去认识化学变化是认识化学的重要手段。实验用品:37%的浓盐酸(密度为1.18g/mL)、10%的氢氧化钠溶液、蒸馏水量筒、温度计。
实验一:配制100mL 10%的盐酸(密度为1.05g/mL)
实验步骤:
(1)计算:需要37%的浓盐酸的体积为______mL(精确到0.01mL,下同):需要蒸馏水的体积为______mL(水的密度为10g/mL)
(2)量取浓盐酸和蒸馏水
(3)混合配制
实验二:在一定体积的10%的氢氧化钠溶液中滴加10%的盐酸(室温下),反应中溶液温度的变化如下:
加入盐酸的体积(V)mL | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 | 18 | 20 |
溶液温度变化(△t)℃ | △t1 | 5.2 | 9.6 | 12.0 | 16.0 | 18.2 | 16.7 | 15.7 | 14.7 | 13.7 | 12.9 |
①表中△t1的值为______。
②写出该反应的化学方程式______。
③当加入盐酸的体积为10mL时,所得溶液的溶质一定含有______。
④根据上表分析,加入盐酸的体积在0~10mL,溶液温度变化的趋势及其原因是______。
⑤其他条件不变,若改用20%的盐酸进行滴加,结合对上述曲线的分析,大胆猜想新曲线最高点的位置(不考虑溶液密度和比热容的变化及热量散失等影响因素)______

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是常见固体物质的溶解度曲线,根据图示回答:
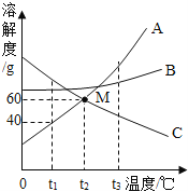
(1)t3℃时,A、B、C三种物质的溶解度由大到小的顺序为____。
(2)t1℃时,将20g A物质放入100g水中,充分溶解后所得的溶液是____(填“饱和”或“不饱和”)溶液.欲使t2℃时C物质的饱和溶液变为不饱和溶液,可采取的方法是___(任填一种方法)。
(3)现有30℃的不饱和KNO3溶液,与该溶液有关的量有:
①水的质量 ②溶液中KNO3的质量 ③KNO3的质量分数
④30℃时KNO3的溶解度 ⑤溶液的质量
Ⅰ.在该不饱和溶液中加硝酸钾至饱和,不变的量有______(填序号,下同),
Ⅱ.将该不饱和溶液恒温蒸发至饱和,不变的量有_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】学习酸碱中和反应时,很多同学对其产生探究兴趣。
(1)甲同学将固体氢氧化钠放入装有稀硫酸的试管中并振荡,试管壁发烫,于是他得出酸碱中和反应是放热反应的结论。乙同学认为甲同学推理不合理,理由是__________________。
(2)乙同学为了验证甲同学的结论,将实验加以改进:将稀硫酸慢慢滴入装有氢氧化钠溶液的烧杯中,用温度计测出氢氧化钠溶液温度随加入稀硫酸质量的变化如下图:
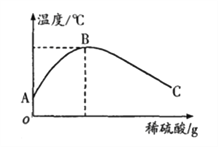
①由图知,稀硫酸与氢氧化钠溶液发生的反应是_________(填“放热”或“吸热”)反应,B点表示的含义是__________________。
②从A到B的过程中,烧杯中溶液pH逐渐 ____________。
③B到C的过程中,烧杯内溶液中含有的阳离子有 ________(填离子符号)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A→I是初中化学常见的物质,它们的相互转化关系如图所示,其中A、B组成元素相同且常温下为液体,C、D、E为无色气体,E为温室气体之一,H是石灰石的主要成分。回答下列问题:
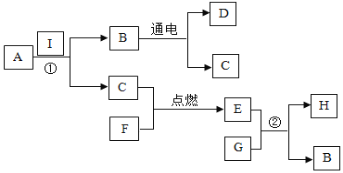
(1)写出下列物质的化学式:D_____;F_____。
(2)写出反应①的化学方程式_____________,基本反应类型为_____。
(3)写出反应②的化学方程式_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是某化学兴趣小组。设计的金属活动性顺序的探究实验。
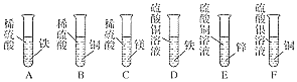
(1)上述实验中,有气泡生成的是________(填写装置序号)。
(2)试管F中出现的实验现象是______________。
(3)上述实验能否证明镁、锌、铁、铜、银五种金属的活动性强弱?____请说明理由_____。
(4)我国古代“湿法炼铜”就是利用了试管D中的反应原理,请写出该反应的化学方程式:______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com