
| 物 质 | 选用的方法或试剂 | |
| A | 空气和二氧化碳 | 燃着的木条 |
| B | 氧气和二氧化碳 | 通入澄清石灰水 |
| C | 硬水和软水 | 肥皂水 |
| D | 酒精和水 | 看颜色 |
| A. | A | B. | B | C. | C | D. | D |
科目:初中化学 来源: 题型:选择题
| A. | 用高锰酸钾制02时,反应试管的管口应略向上倾斜 | |
| B. | 做铁在02中燃烧实验时,集气瓶应先放少量水或细沙 | |
| C. | 铁、锌、碘元素都属于微量元素 | |
| D. | 用金属和酸制H2时,可采用与制C02相同的发生装置 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
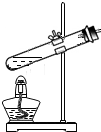 研究和控制化学反应条件有重要意义.同学们想探究双氧水的浓度对反应速率的影响.在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间.
研究和控制化学反应条件有重要意义.同学们想探究双氧水的浓度对反应速率的影响.在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间. | 实验 | 30%双氧水的质量(g) | 加入的水的体积(mL) | 二氧化锰质量(g) | 收集时间(s) |
| 1 | 10 | 40 | 5 | 200 |
| 2 | 20 | 30 | 5 | 100 |
| 3 | 30 | 20 | 5 | 67 |

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
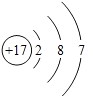 ,在化学反应中容易失去电子的是X元素,两种元素形成的化合物的化学式是XY2(可用X、Y表示,也可以用元素符号表示)
,在化学反应中容易失去电子的是X元素,两种元素形成的化合物的化学式是XY2(可用X、Y表示,也可以用元素符号表示)查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com