
 欲测定铜镁合金的组成(其他元素忽略不计),进行如下实验:取铜镁合金20g放入烧杯,将200g稀硫酸分4次加入烧杯中,充分反应后,测得剩余固体的质量记录如下:
欲测定铜镁合金的组成(其他元素忽略不计),进行如下实验:取铜镁合金20g放入烧杯,将200g稀硫酸分4次加入烧杯中,充分反应后,测得剩余固体的质量记录如下:| 次数 | 1 | 2 | 3 | 4 |
| 加入稀硫酸质量/g | 50 | 50 | 50 | 50 |
| 剩余固体质量/g | 17.6 | 15.2 | m | 14 |
分析 铜镁合金中镁能与稀硫酸反应生成硫酸镁和氢气,铜不与稀硫酸反应,由表格第1次、第2次数据分析可知,50g稀硫酸能与2.4g镁恰好完全反应,第2次到第4次,固体质量减少1.2g,说明第3次加入的稀硫酸后,镁已经完全反应;由参加反应的镁的质量,由反应的化学方程式列式计算出硫酸的质量,进一步计算所加稀硫酸的溶质的质量分数.根据参加反应的镁的质量,由反应的化学方程式列式计算出氢气的质量和硫酸的质量,之后作图.
解答 解:(1)铜镁合金中镁能与稀硫酸反应生成硫酸镁和氢气,铜不与稀硫酸反应,由表格第1次、第2次数据分析可知,50g稀硫酸能与2.4g镁恰好完全反应,第2次到第4次,固体质量减少1.2g,说明第3次加入的稀硫酸后,镁已经完全反应,硫酸过量,剩余固体为铜,所以m=14.
合金中铜、镁的质量最简比是14g:(20g-14g)=7:3.故填:14;7:3;
(2)第1次实验参加反应的镁的质量为20g-17.6g=2.4g.
设消耗硫酸的质量为x
Mg+H2SO4═MgSO4+H2↑
24 98
2.4g x
$\frac{24}{2.4g}=\frac{98}{x}$
x=9.8g.
所加稀硫酸的溶质的质量分数为$\frac{9.8g}{50g}×100%$=19.6%,
(3)参加反应的镁的质量为20g-14g=6g.
设反应结束后生成氢气的质量为y,共消耗稀硫酸的质量为z,
Mg+H2SO4═MgSO4+H2↑
24 98 2
6g z×19.6% y
$\frac{24}{6g}=\frac{98}{z×19.6%}=\frac{2}{y}$
y=0.5g,z=125g
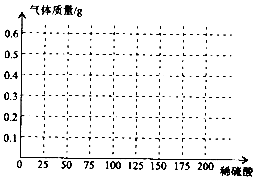
所以加入稀硫酸与产生气体关系的曲线图为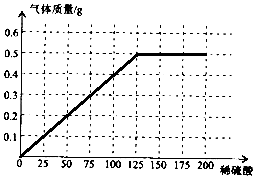 .
.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,细致地分析图表信息,确定50g稀硫酸能与2.4g镁恰好完全反应是正确解答本题的前提和关键.


科目:初中化学 来源: 题型:实验探究题
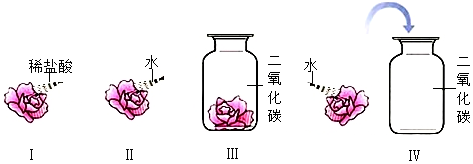
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | HC1 | B. | NaCl | C. | Na2CO3 | D. | FeSO4•7H2O |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 |
| NH4C1溶解度/g | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
| NaCl溶解度/g | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
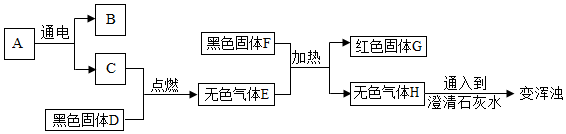
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
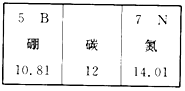
| A. | 碳元素对应原子的质子数为12 | |
| B. | 碳元素属于非金属元素 | |
| C. | 含有碳元素的化合物都是有机化合物 | |
| D. | 由碳元素组成的单质化学性质活泼 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com