
 2012年“世界水日”的宣传主题是水与链式安全,水是生命之源,我们应该水,爱护水资源.某化学兴趣小组对某地水质状况进行了相关研究调查:
2012年“世界水日”的宣传主题是水与链式安全,水是生命之源,我们应该水,爱护水资源.某化学兴趣小组对某地水质状况进行了相关研究调查: 2H2↑+O2↑.
2H2↑+O2↑. 2H2O+O2↑
2H2O+O2↑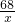
 ×100%=2%.
×100%=2%.

 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
 (2012?贵港)2012年“世界水日”的宣传主题是“水与粮食安全”,水与生活生产有着密切关系,但今年1月15日,广西龙江河河段检测出重金属镉含量超标,严重威胁沿岸及下游居民饮水的安全.
(2012?贵港)2012年“世界水日”的宣传主题是“水与粮食安全”,水与生活生产有着密切关系,但今年1月15日,广西龙江河河段检测出重金属镉含量超标,严重威胁沿岸及下游居民饮水的安全.查看答案和解析>>
科目:初中化学 来源: 题型:
| A、水是生命之源、生产之要、生态之基 | B、保护植被、涵养水源、防治水土流失 | C、合理开发利用,重在节约保护 | D、淡水资源丰富,可以任意使用 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com