
【题目】下图是用红磷燃烧法来测定空气中氧气的体积分数的实验。
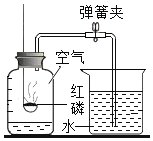
(1)写出红磷在空气中燃烧的符号表达式_____;
(2)实验前在集气瓶内加入少量水,将集气瓶上方空气分成五等份,并做好记号。红磷熄灭并冷却至室温后,打开弹簧夹,此时可观察到的现象为_____;
(3)如果未等到装置冷却到室温就打开弹簧夹,测得的结果会_____(填“偏大”或“偏小”或“无影响”);
(4)能否用蜡烛代替红磷实验:_____(填“能”或“否”),理由是_____;
(5)我们知道,另有两种物质在氧气中燃烧的实验中也应先向集气瓶中加少量水。请写出加水的目的为吸收有害物质、减少空气污染的可燃物的名称_____。
【答案】P+O2![]() P2O5 红磷燃烧,产生大量白烟,放出大量的热,烧杯中的水进入集气瓶内,约占集气瓶内空气气体的
P2O5 红磷燃烧,产生大量白烟,放出大量的热,烧杯中的水进入集气瓶内,约占集气瓶内空气气体的![]() 偏小 不能 蜡烛燃烧,反应物为气体氧气,生成的产物是二氧化碳气体,瓶内压强变化不大,不能测出空气中氧气的含量 硫
偏小 不能 蜡烛燃烧,反应物为气体氧气,生成的产物是二氧化碳气体,瓶内压强变化不大,不能测出空气中氧气的含量 硫
【解析】
(1)红磷与氧气反应生成五氧化二磷,反应的符号表达式为:P+O2![]() P2O5;
P2O5;
(2)红磷燃烧来测定空气中氧气的含量,空气中氧气的体积含量约占![]() ,发生的实验现象是:红磷燃烧,产生大量白烟,放出大量的热; 烧杯中的水进入集气瓶内,约占集气瓶内空气气体的
,发生的实验现象是:红磷燃烧,产生大量白烟,放出大量的热; 烧杯中的水进入集气瓶内,约占集气瓶内空气气体的![]() ;
;
(3)如果红磷熄灭后没有完全冷却到室温就打开弹簧夹,实验结果会偏低,其原因是:与室温相比,剩余气体温度较高,压强偏大,因此进入集气瓶中的水偏少;
(4)不能用蜡烛代替红磷测定空气中氧气的含量,原因是:蜡烛燃烧,反应物为气体氧气,生成的产物是二氧化碳气体,瓶内压强变化不大,不能测出空气中氧气的含量。
(5)硫在氧气中燃烧生成二氧化硫刺激性气体,故硫在氧气中燃烧的实验中也应先向集气瓶中加少量水来吸收有害物质、减少空气污染。


科目:初中化学 来源: 题型:
【题目】实验课上,同学们利用下列装置进行气体制备的学习。请回答下列问题:
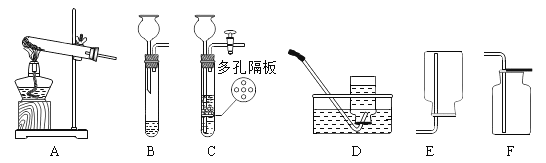
(1)用装置A制取O2的化学方程式为_________________;
(2)装置B或C均可用于实验室制取氢气,与装置B相比,装置C的优点是_________________;
(3)实验室可用装置D、E或F收集气体,收集O2和CO2都能用的装置是_________________。(填序号)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】走进超市,亮亮同学来到食品区发现一些包装袋内充满了气体,看上去好像一个小“枕头”。

(1)薯片的主要成分有土豆、盐等,属于_____ (填“纯净物”或“混合物”)。
(2)填充气体的主要作用是______。
(3)你认为食品充气包装,对所充气体的要求是(回答两点即可):①______;②_______。
(4)薯片暴露在空气中一段时间后,会发现变软了,说明空气中含有_______。
(5)淇淇同学对所填充的气体提出两种猜想:①氮气:②二氧化碳。请你设计一个实验验证猜想②,则所需要的仪器有______(填序号)。
A 小试管 B 注射器 C 量筒 D 小烧杯
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为区別N2、H2、CO2、CH4四种气体,小丽进行了下面实验:
①点燃四种气体,将气体分为可燃性气体和不可燃性气体;
②在可燃性气体火焰上方,分別罩一内壁附有澄清石灰水的烧杯,烧杯内壁出现白色浑浊的是气体Ⅰ,无明显变化的是气体Ⅱ;
③将不可燃性气体通入澄清石灰水,其中,能使澄清石灰水变浑浊的是气体Ⅲ,无明显变化的是气体Ⅳ。根据实验推断,Ⅰ、Ⅱ、Ⅲ、Ⅳ对应的气体分别是( )
A. ![]() 、
、![]() 、
、![]() 、
、![]() B.
B. ![]() 、
、![]() 、
、![]() 、
、![]()
C. ![]() 、
、![]() 、
、![]() 、
、![]() D.
D. ![]() 、
、![]() 、
、![]() 、
、![]()
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了测定某品牌食用纯碱中碳酸钠的质量分数,小明取10克食用纯碱样品和足量的溶质质量分数为10%的稀硫酸,进行如图甲实验,实验前后,均需往装置中缓慢通一会儿氮气.(样品中其他成分不与稀硫酸反应)
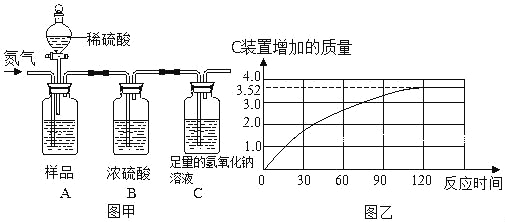
(1)实验前,先往A装置通入一会儿氮气的目的是_____.
(2)随着纯碱样品与稀硫酸反应,C装置增加的质量变化情况如图乙所示,则该食用纯碱中碳酸钠的质量分数是多少___________?
(3)若将稀硫酸换为浓盐酸,实验中C装置增加的质量会偏大,请说明理由_________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图中用“![]() ”表示反应的方向,用“—”表示连线两端的物质能够发生化学变化。现已知A是红棕色固体,B存在于人体胃液中,C是一种气体单质,F常用于配制波尔多液,他们之间的部分转换关系见图(部分反应物生成物省略)。
”表示反应的方向,用“—”表示连线两端的物质能够发生化学变化。现已知A是红棕色固体,B存在于人体胃液中,C是一种气体单质,F常用于配制波尔多液,他们之间的部分转换关系见图(部分反应物生成物省略)。
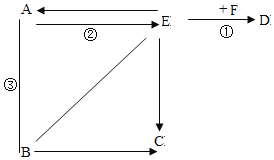
(1)B的化学式为_______。
(2)反应①的基本反应类型是_______,反应②的条件是________。
(3)反应③的化学方程式______,其在生产生活中可用于________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业上以废旧锌锰电池中的黑锰粉[MnO2、MnO(OH)、NH4Cl、少量ZnCl2、炭黑及氧化铁等]为原料制备MnCl2,实现锰的再利用。其工艺流程如下:
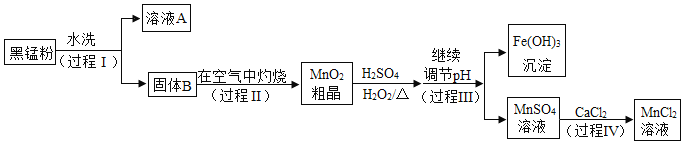
(1)过程Ⅰ、Ⅲ、Ⅳ中都需要的操作为______________。
(2)溶液A中的溶质除了NH4Cl,还含有____________(填化学式) 。
(3)过程Ⅱ的目的是除炭、氧化MnO(OH),其产物为三种常见氧化物,除CO2外,另外两种物质的化学式为______________。
(4)查阅资料:在pH>a的溶液中,Fe3+会转化成氢氧化铁沉淀,在pH>b的溶液中,Mn2+会转化成氢氧化锰沉淀。结合过程Ⅲ分析,可推测a_______b (填“>”、“<”或“=”)。
(5)结合复分解反应的条件和表中信息:过程IV的化学方程式为____________________。
MnSO4 | CaCl2 | MnCl2 | CaSO4 | |
溶解性 | 易溶 | 易溶 | 易溶 | 微溶 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】做电解水实验时,常在水中加入氢氧化钠以增强溶液的导电性,但氢氧化钠本身不会在电解水的过程中发生化学变化,氢氧化钠的质量也不会发生改变。现将8g氢氧化钠的溶液在101g水中并通电,一段时间后生成1g氢气。请回答下列问题:
(1)当生成0.7g氢气时,氢气与氧气在相同条件下的体积比约为_______;
(2)电解过程中,生成1g氢气时所消耗的水的质量为_______g;
(3)电解水过程中,当生成1g氢气时水溶液中氢氧化钠的质量分数为_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙三种固体物质的溶解度曲线如图所示,从中获取的信息正确的是( )
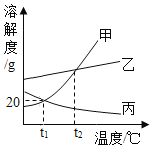
A.升高温度可使丙的饱和溶液变为不饱和溶液
B.t2℃乙、丙两种溶液所含溶质的质量一定不同
C.t1℃甲、丙饱和溶液的溶质质量分数均为16.7%
D.t2℃甲、乙、丙的饱和溶液降温至t1℃,所得溶液的溶质质量分数大小顺序为乙>甲=丙
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com