
(2分)将一定量的铜粉投入稀硫酸中无现象,滴加H2O2,铜逐渐溶解,溶液变蓝色但无气泡生成,则方程式为 ;待铜溶解完,再滴加H2O2,有气泡产生,则方程式为 。
科目:初中化学 来源:2013-2014江苏省太仓市九年级5月学科教学质量调研化学试卷(解析版) 题型:选择题
某溶液中含n个K+,n个SO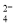 ,n个Cl-,除存在不等数目的H+和OH-外,别无其它离子存在,请你推测此溶液
,n个Cl-,除存在不等数目的H+和OH-外,别无其它离子存在,请你推测此溶液
A.pH>7 B.pH=7 C.pH<7 D.pH≥7
查看答案和解析>>
科目:初中化学 来源:2013-2014江苏省大丰市第二次调研考试化学试卷(解析版) 题型:选择题
在学习化学的过程中,我们会发现许多具有规律性的知识。下列叙述中不正确的是()
A.对难溶于水的气体可用排水集气法收集 B.碱溶液中都含有相同的OH—
C.含氢元素的物质完全燃烧会产生水 D.金属都能与酸反应产生氢气
查看答案和解析>>
科目:初中化学 来源:2013-2014江苏省大丰市九年级第一次调研考试化学试卷(解析版) 题型:选择题
《舌尖上的中国》主要介绍中国的美食及其制作方法。“饮食健康”是人们普遍的生活追求,下列做法正确的是
A.用甲醛浸泡海产品
B.在煲好的鸡汤中放入适量的加碘食盐
C.在果汁中加入“塑化剂”使其口感更好
D.在香肠中添加过量的亚硝酸钠使其保持肉质鲜美
查看答案和解析>>
科目:初中化学 来源:2013-2014江苏省句容市九年级下学期一模化学试卷(解析版) 题型:探究题
(14分)某校化学兴趣小组欲对食盐的用途进行探究,获得以下信息并对相关问题进行研究。
一、用途之一:作调味品。
食盐的主要成份是NaCl, 通过晾晒海水或煮盐井水、盐湖水等,可以蒸发除去水分得到粗盐.粗盐中含有难溶性杂质(泥沙等)和多种可溶性杂质(氯化镁、氯化钙等).
[提出问题]如何才能将粗盐中难溶性杂质和可溶性杂质(氯化镁、氯化钙)除去,从而获得较纯的食盐晶体?
[资料准备]
20℃时,一些物质的溶解度 | ||
| OH- | CO32- |
Na+ | 溶 | 溶 |
Ca2+ | 微 | 不 |
Mg2+ | 不 | 微 |

[实验方案]某同学为了提纯粗盐,设计了如下实验方案并进行实验.
[交流与表达]
(1)实验操作X的名称是 ,该操作中要用到的玻璃仪器有烧杯、玻璃棒和 。
(2)实验步骤③的主要目的是 (用化学方程式回答);判断氢氧化钠溶液已过量的方法是 。
(3)有同学认为原实验方案不完善,做出这种评价的依据是 。
二、用途之二:制备氯气。
工业上用电解饱和食盐水来制备氯气,可以得到多种化工产品,除氯气(Cl2)外,还生成密度最小的气体,向反应后的溶液中滴加无色酚酞试液,溶液变红,请写出发生反应的化学方程式 。
三、用途之三:工业制碱。
某厂采用“侯氏制碱法”生产化工产品——纯碱(Na2CO3)和化肥NH4Cl。
【相关资料】
⑴ NH4Cl△NH3↑+HCl↑
⑵已知20℃时有关物质的溶解度如下(气体指1体积水中能溶解的气体体积)
物质 | NaCl | NaHCO3 | NH4Cl | NH3 | CO2 |
溶解度 | 36.0g | 9.6g | 37.2g | 710 | 0.9 |
【生产原理】是:将NH3和CO2通入饱和食盐水中得到NaHCO3和NH4Cl的混合物,反应的化学方程式为: ;分离出NaHCO3,加热制得纯碱。
【生产流程】如下
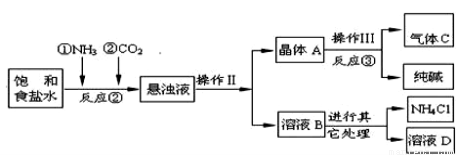
【问题讨论】:
(1)反应③中得到纯碱的化学方程式为: 。
(2)检验气体C的方法 。
(3)在反应②中,先通 气体,目的是 。
【组成确定】
(1)称取一定质量的纯碱样品,经多次充分加热后,再称重,质量无变化;
(2)另取少量纯碱样品加入适量水,样品完全溶解,向该溶液中加入过量稀HNO3,再滴加AgNO3溶液,有白色沉淀。由上述实验可确定纯碱样品含有杂质 (写化学式)。
【含量测定】
称取纯碱样品10.8g加入适量水,再加入过量CaCl2溶液,搅拌、过滤、洗涤、干燥后称得固体质量为10.0g,请通过计算判断此纯碱样品的纯度为 。(保留一位小数)
【总结反思】
某同学认为,在上述纯碱含量测定中,将CaCl2溶液改为BaCl2溶液,测定误差会减小,其理由是 。
查看答案和解析>>
科目:初中化学 来源:2013-2014江苏省句容市九年级下学期一模化学试卷(解析版) 题型:选择题
下图为某化工企业生产流程示意图,下列说法正确的是
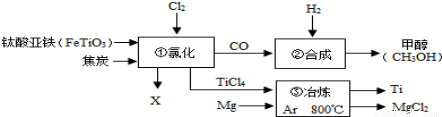
A.钛酸亚铁(FeTiO3)中钛元素为+3价
B.①中反应为:2FeTiO3+6C+7Cl2一定条件2X+2TiCl4+6CO,则X为FeCl2
C.③中氩气(Ar)作保护气,反应类型为置换反应
D.②中为使原料全部转化为甲醇,理论上CO和H2投料的质量比为1:2
查看答案和解析>>
科目:初中化学 来源:2013-2014江苏省句容市九年级下学期一模化学试卷(解析版) 题型:选择题
把Cu、Zn的混合物放入一定量的硝酸银溶液中,使其充分反应后过滤,得到固体和蓝色滤液。下列说法正确的是
A. 滤出的固体中一定含有银,可能含有铜
B.滤出的固体中一定含有银和铜,可能含有锌
C.滤液中一定含有硝酸铜,一定没有硝酸锌和硝酸银
D.滤液中一定含有硝酸锌、硝酸铜、硝酸银
查看答案和解析>>
科目:初中化学 来源:2013-2014江苏省南通市通州区中考适应性考试化学试卷(解析版) 题型:填空题
(5分)在宏观、微观和符号之间建立联系是学习化学的基本方法。
(1)下列为A、B、C、D的原子或离子的结构示意图。
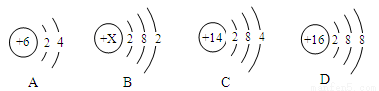
①B的原子结构示意图中X为 ;若D的元素符号为S,则D表示的微粒符号是 。
②分析A、C的原子结构,你认为A与C具有相似化学性质的原因是 。
(2)下图为处理汽车尾气化学反应微观示意图,其中A、B、C、D表示4种物质,A和B在一定条件下反应可生成C 和D。
反应前 | 反应后 |
| ||
|
|
|
| |
|
|
|
| |
③物质C中,各元素的质量比为 。
④根据上述微观示意图,处理汽车尾气的化学反应方程式为 。
查看答案和解析>>
科目:初中化学 来源:2013-2014江苏省南京市鼓楼区中考二模化学试卷(解析版) 题型:探究题
学习了金属的化学性质后,某兴趣小组进行了如下实验:将足量镁条加入到氯化铜溶液 中,观察到镁条表面有气泡产生,同时有红色固体附在镁条表面。
【提出问题】产生气体是什么物质? 有红色固体又是什么物质?
【查阅资料】在金属活动性顺序里,位于氢后面的金属Cu,在常温下虽然不能与稀盐酸、稀硫酸反应,但可以与稀硝酸反应,其化学方程式为:
3Cu+8HNO3(稀)=3Cu(NO3)2+2NO ↑ +4H2O
反应生成的NO是无色、难溶于水的气体,在常温下与空气中的O2迅速化合生成 N02,N02是红棕色、有刺激性气味的有毒气体。
【作出猜想】猜想一:气体可能是氢气、红色固体是金属氧化铁;猜想二:气体可能是氢气、 红色固体是金属铜;猜想三:气体可能是二氧化碳、红色固体是金属铜。
【交流讨论】大家思考后,一致认为猜想一和三不合理,其理由是_____________________。
【实验与结论】
实验步骤 | 现象 | 结论 |
(1)取少量红色固体于一支洁净的试管中,加入稀盐酸 | __________________________________ | 猜想一不成立
|
(2)①用尖嘴导管将气体导出并引燃,同时在上方放一块干冷的玻璃片 ②取少量红色固体于一支洁净的试管中,加入稀硝酸 | 该气体能燃烧,且玻璃片上有______出现 红色固体溶解,得到蓝色溶液同时看到试管上部有红棕色气体产生 | 猜想二成立 |
【继续探究】
(1)用pH试纸测得氯化铜溶液pH约为4,说明氯化铜溶液中含有较多的________离子。
(2)取7.68g 红色固体,加入100g稀HNO3溶液,如恰好完全反应,计算生成NO的质量(化学方程式见上)和反应前稀HNO3溶液中溶质的质量分数。 (请写出计算过程)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com