
”¾ĢāÄæ”æKNO3”¢NaNO3”¢NaClČżÖÖĪļÖŹµÄČܽā¶ČĒśĻßČēĻĀĶ¼ĖłŹ¾£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
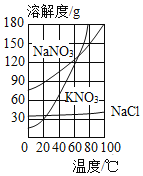
A.KNO3µÄČܽā¶Č±ČNaCl“ó
B.½«KNO3±„ŗĶČÜŅŗ½µĪĀ£¬ČÜŅŗÖŠKNO3µÄÖŹĮæ·ÖŹż²»±ä
C.KNO3±„ŗĶČÜŅŗÖŠŗ¬ÉŁĮæNaCl£¬æÉĶعż½µĪĀ½į¾§µÄ·½·ØĢį“æ
D.100g40”ęNaNO3µÄ±„ŗĶČÜŅŗ½µĪĀÖĮ0”ę£¬Īö³öNaNO3¹ĢĢå31g
”¾“š°ø”æC
”¾½āĪö”æ
A”¢ÓÉӌƻӊÖøĆ÷ĪĀ¶Č£¬ĪŽ·Ø±Č½ĻČܽā¶Č“󊔣¬¹ŹŃ”Ļī“ķĪó£»
B”¢KNO3Čܽā¶Č»įĖę×ÅĪĀ¶ČµÄ½µµĶ¶ų¼õŠ”£¬½«KNO3±„ŗĶČÜŅŗ½µĪĀ£¬»įÓŠ¾§ĢåĪö³ö£¬ČÜŅŗÖŠKNO3µÄÖŹĮæ·ÖŹż±äŠ”£¬¹ŹŃ”Ļī“ķĪó£»
C”¢KNO3Čܽā¶Č»įĖę×ÅĪĀ¶ČµÄ½µµĶ¶ų¼õŠ”£¬ĀČ»ÆÄʵÄČܽā¶ČŹÜĪĀ¶Č±ä»ÆÓ°Ļģ½ĻŠ”£¬ĖłŅŌKNO3±„ŗĶČÜŅŗÖŠŗ¬ÉŁĮæNaCl£¬æÉĶعż½µĪĀ½į¾§µÄ·½·ØĢį“棬¹ŹŃ”ĻīÕżČ·£»
D”¢Čܽā¶ČŹĒÖøŅ»¶ØĪĀ¶ČĻĀ£¬100gČܼĮµÄĄļ×ī¶ąČܽāµÄČÜÖŹÖŹĮ棻40”ęµÄNaNO3±„ŗĶČÜŅŗ½µĪĀÖĮ0”ę£¬Čܽā¶ČµÄ±ä»ÆĪŖ104g-73g=31g£¬¼“ŗ¬ÓŠ100gČܼĮĖ®µÄNaNO3±„ŗĶČÜŅŗÓÉ40”ęµÄ½µĪĀÖĮ0”ę£¬×ī¶ąĪö³ö31gĻõĖįÄĘ£¬100gNaNO3µÄ±„ŗĶČÜŅŗĪö³öµÄÖŹĮæ±ŲŠ”ÓŚ31g£¬¹ŹŃ”Ļī“ķĪ󔣹ŹŃ”C”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ(5·Ö) ĻĀĶ¼ŹĒŹµŃéŹŅ³£ÓƵÄ×°ÖĆ”£Ēė¾ŻĶ¼»Ų“š£ŗ
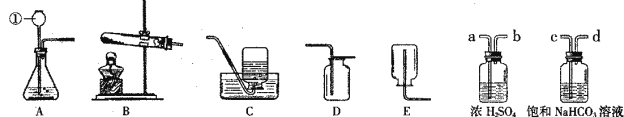
£Ø1£©Š“³öŅĒĘ÷¢ŁµÄĆū³Ę ”£ŹÕ¼ÆijĘųĢåÖ»ÄܲÉÓĆE×°ÖĆ£¬ÓÉ“ĖĶĘ²āøĆĘųĢå¾ßÓŠµÄŠŌÖŹ £»
£Ø2£©ÓĆøßĆĢĖį¼ŲÖĘČ”ŃõĘųµÄ×°ÖĆ×éŗĻŹĒ £ØĢīŠņŗÅ£©£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ £»
£Ø3£©ŹµŃéŹŅÖʵƵÄCO2ĘųĢåÖŠ³£ŗ¬ÓŠHClŗĶĖ®ÕōĘų”£ĪŖĮĖµĆµ½“æ¾»”¢øÉŌļµÄCO2ĘųĢ壬³żŌÓ×°ÖƵĵ¼¹ÜĘųĮ÷·½ĻņĮ¬½ÓĖ³ŠņŹĒ £ØĢīŃ”Ļī£©”£
A£®a”śb”śc”śd B£®b”śa”śc”śd
C£®c”śd”śa”śb D£®d”śc”śb”śa
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æN95æŚÕÖµÄ×ī“óĢŲµć¾ĶŹĒæÉŅŌŌ¤·ĄÓÉ»¼ÕßĢåŅŗ»ņŃŖŅŗ·É½¦ŅżĘšµÄ·ÉÄ“«Č¾”£ÄÜÓŠŠ§µÄ±£ÕĻČĖĢ彔浔£ĻĀĶ¼ŹĒijN95æŚÕֵĽį¹¹Ķ¼”£Ēė»Ų“š£ŗ

£Ø1£©Ķ¼ÖŠ±źŹ¾ĪļÖŹŹōÓŚ½šŹō²ÄĮĻµÄŹĒ_____£ØĢīŅ»øö¼“æÉ£¬ĻĀĶ¬£©£»ŹōÓŚÓŠ»śŗĻ³É²ÄĮĻµÄ_____”£
£Ø2£©ĀĮŗĻ½šÄĶ”¢øÆŹ“µÄŌŅņŹĒ_____”££ØÓĆ»Æѧ·½³ĢŹ½±ķŹ¾£©
£Ø3£©ĆŽ»ØÓėŃņĆ«ČēŗĪĒų·Ö_____”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”湤ŅµÉś²ś“æ¼īÖŠ³£ŗ¬ÓŠÉŁĮæ NaCl ŌÓÖŹ£¬ĻČ³ĘČ” 12g “æ¼īѳʷ·ÅČėÉÕ±ÖŠ£¬¼ÓČė100g Ė®Ź¹ĘäĶźČ«Čܽā£¬ĻņĘäÖŠ²»¶ĻµĪ¼ÓĀČ»ÆøĘČÜŅŗ£¬²āµĆ¼ÓČėĀČ»ÆøĘÖŹĮæÓėÉś³É³ĮµķÖŹĮæČēĶ¼ĖłŹ¾”£

£Ø1£©ŃłĘ·ÖŠĢ¼ĖįÄʵÄÖŹĮæ ”£
£Ø2£©a µćŹ±£¬¶ŌÓ¦ČÜŅŗÖŠČÜÖŹÓŠ ”£
£Ø3£©ŹŌ¼ĘĖćĒ”ŗĆĶźČ«·“Ó¦Ź±£¬·“Ó¦ŗóČÜŅŗÖŠČÜÖŹµÄÖŹĮæ·ÖŹż”££Ø¾«Č·µ½ 0.1%£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æøł¾ŻČēĶ¼ĖłŹ¾×°ÖĆ£¬»Ų“šÓŠ¹ŲĪŹĢā£ŗ
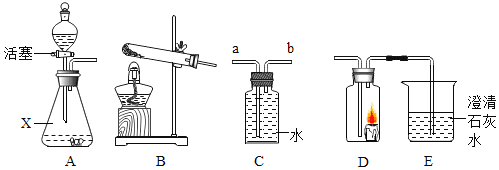
£Ø1£©×°ÖĆAÖŠ£¬ŅĒĘ÷XµÄĆū³ĘĪŖ______£¬ĘäÖŠÓĆ·ÖŅŗĀ©¶·“śĢę³¤¾±Ā©¶·µÄÓŵćŹĒ______”£
£Ø2£©ŹµŃéŹŅ³£ÓĆĀČĖį¼ŲÖĘČ”ŃõĘų£¬·¢Éś×°ÖĆӦєŌń______![]() Ģī×ÖÄø
Ģī×ÖÄø![]() £¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ______
£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ______
£Ø3£©ČōÓĆ×°ÖĆCŹÕ¼ÆĒāĘų£¬ŌņĒāĘųÓ¦“Ó______![]() Ģī”°a”±»ņ”°b”±
Ģī”°a”±»ņ”°b”±![]() ¶Ėµ¼¹ÜæŚĶØČė”£
¶Ėµ¼¹ÜæŚĶØČė”£
£Ø4£©ŅŅČ²ŹĒŅ»ÖÖĪ¢ČÜÓŚĖ®µÄĘųĢ壬ĆܶČÓėæÕĘų½Ó½ü£¬ŹµŃéŹŅ³£ÓĆæéדµēŹÆŗĶĖ®ŌŚ³£ĪĀĻĀ·“Ó¦ÖĘČ”ŅŅČ²£¬¹ŹÖĘČ”ŅŅČ²µÄ·¢Éś×°ÖĆŃ”______”£![]() Ģī×°ÖĆŠņŗÅ
Ģī×°ÖĆŠņŗÅ![]()
£Ø5£©Ä³Ķ¬Ń§µćČ¼ĄÆÖņ£¬Č»ŗó·ÅČėDÖŠ£¬ŃøĖŁĮ¬½ÓA”¢D”¢E£¬“ņæŖ»īČū½ųŠŠŹµŃ飬·¢ĻÖEÖŠČÜŅŗÖš½„±ä»ė×Ē£¬Ōņ×°ÖĆAÖŠ²śÉśµÄĘųĢå______”£![]() Ģī”°Ņ»¶Ø”±»ņ”°²»Ņ»¶Ø”±
Ģī”°Ņ»¶Ø”±»ņ”°²»Ņ»¶Ø”±![]() ĪŖ¶žŃõ»ÆĢ¼ĘųĢ唣
ĪŖ¶žŃõ»ÆĢ¼ĘųĢ唣
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČĖĄąÉē»įµÄ·¢Õ¹Ąė²»æŖ½šŹō”£ĒėŅĄ¾ŻĖłŃ§ÖŖŹ¶ĢīæÕ”£
£Ø1£©Ä³ŗĻ½šÖŠŗ¬ÓŠ½šŹōīÖ£ØSc£©”£ĻąĶ¬Ģõ¼žĻĀ£¬Č”ĻąĶ¬×“Ģ¬µÄ½šŹōīÖŗĶŠæ·Ö±šÓėĻąĶ¬ÖŹĮæ·ÖŹżµÄŃĪĖį·“Ó¦£¬īÖ²śÉśĘųÅŻĖŁĀŹĆ÷ĻŌøüæģ£¬ŌņScÓėZnµÄ½šŹō»ī¶ÆŠŌĖ³ŠņŹĒ_____”£ŅŃÖŖScÓėĻ”ŃĪĖį·¢ÉśÖĆ»»·“Ó¦£¬Éś³É+3¼Ū»ÆŗĻĪļ£¬Š“³öøĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½_____”£
£Ø2£©µĶĪĀĻĀŌŚČÜŅŗÖŠæÉÖʵĆĒāŃõ»ÆŅų°×É«³Įµķ”£³£ĪĀĻĀĒāŃõ»ÆŅų¼«²»ĪČ¶Ø£¬Ņ×·Ö½āĪŖ×ŲŗÖÉ«ÄŃČÜÓŚĖ®µÄŃõ»ÆŅų¹ĢĢ唣½«AgNO3ČÜŅŗÓėNaOHČÜŅŗŌŚµĶĪĀĢõ¼žĻĀ»ģŗĻ£¬³ä·Ö·“Ó¦ŗóŌŁ½«»ģŗĻĪļ±äĪŖ³£ĪĀ”£Õūøö¹ż³ĢÖŠµÄÖ÷ŅŖŹµŃéĻÖĻóŹĒ_____£¬·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ_____”¢_____”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĮņĖį”¢ŃĪĖįŹĒÖŲŅŖµÄ»Æ¹¤ŌĮĻ.
£Ø1£©Š“³öĻ”ĮņĖįÓėĻĀĮŠĪļÖŹ·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ
¢ŁÓėĢś·Ū·“Ó¦£ŗ_____”£
¢ŚÓėĢ¼ĖįÄĘČÜŅŗ·“Ó¦£ŗ_________”£
¢ŪÓėĀČ»Æ±µČÜŅŗ·“Ó¦£ŗ_________”£
¢ÜÓėŃõ»ÆĢś·“Ó¦£ŗ________”£
ÉĻŹö·“Ó¦ÖŠ£¬²»ŹōÓŚĖįµÄ¹²Ķ¬ŠŌÖŹµÄŹĒ£ØĢī±ąŗÅ£©_________”£
£Ø2£©ŃĪĖįµÄĻĀĮŠÓĆĶ¾ÖŠ£¬²»ÄÜÓĆĮņĖį“śĢęŃĪĖįµÄŹĒ £ØĢī±ąŗÅ£©_____”£
¢Ł½šŹō±ķĆę³żŠā ¢ŚÖĘŌģŅ©ĪļĀČ»ÆŠæ ¢Ū³żČ„ NaCl ÖŠµÄÉŁĮæ NaOH£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æij»ÆѧŠĖȤŠ”×éµÄĶ¬Ń§ĒåĄķŹµŃéŹŅŹ±·¢ĻÖŅ»ĘæŅŅ“¼ŹŌ¼Į£¬±źĒ©ČēĶ¼”£

£Ø1£©C2H5OHÖŠĢ¼ŌŖĖŲŗĶĒāŌŖĖŲµÄÖŹĮæ±ČĪŖ________(ÓĆ×ī¼ņÕūŹż±Č±ķŹ¾)”£
£Ø2£©ÕāĘæŅŅ“¼ŹŌ¼ĮµÄÖŹĮæĪŖ_______g”£
£Ø3£©ĻÖŅŖÅäÖĘ2000 gČÜÖŹµÄÖŹĮæ·ÖŹżĪŖ40%µÄŅŅ“¼ČÜŅŗ£¬ŠčŅŖŅŅ“¼ŹŌ¼ĮµÄÖŹĮæĪŖ_______g£¬ŠčŅŖÕāÖÖŅŅ“¼ŹŌ¼Į_____Ę攣
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÅšÄąÖ÷ŅŖÓÉMgO ŗĶSiO2 ×é³É£¬ŗ¬ÓŠÉŁĮæFe2O3 ”¢FeO ”¢Al2O3 µČŌÓÖŹ”£ÓĆÅšÄąÉś²śĒāŃõ»ÆĆ¾µÄ¹¤ŅÕĮ÷³ĢČēĶ¼ĖłŹ¾£ŗ
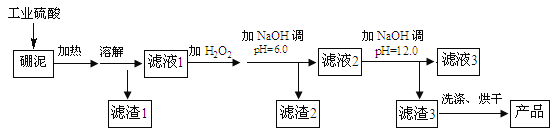
ĢįŹ¾ŠÅĻ¢£ŗ
¢ń£®¼ÓČėH2O2µÄÄæµÄŹĒ½«ČÜŅŗÖŠ Fe2+Ńõ»ÆĪŖ Fe3+
¢ņ£®SiO2²»ÓėĮņĖį·“Ó¦
¢ó£®ŅŃÖŖijŠ©½šŹōŃōĄė×ÓŌŚČÜŅŗÖŠÉś³ÉĒāŃõ»ÆĪļ³ĮµķµÄpHČēĻĀ±ķĖłŹ¾£¬µ±ČÜŅŗµÄpH“ļµ½ĶźČ«³ĮµķÖµŹ±£¬æÉŅŌČĻĪŖ½šŹōŃōĄė×ÓŅŃĶźČ«³Įµķ”£
ĒāŃõ»ÆĪļ | ĶźČ«³ĮµķŹ±µÄpH |
Mg(OH)2 | 10.8 |
Fe(OH)2 | 9.6 |
Fe(OH)3 | 3.7 |
Al(OH)3 | 4.7 |
£Ø1£©Š“³ö¼ÓČČČܽāÖŠ·¢Éś·“Ó¦µÄĘäÖŠŅ»øö»Æѧ·½³ĢŹ½£ŗ____”£
£Ø2£©ĀĖŅŗ2ÖŠ“óĮæ“ęŌŚµÄ½šŹōĄė×ÓŹĒ___”£
£Ø3£©µ÷½ŚĮ½“ĪpHÖµµÄŌŅņŹĒ___”£
£Ø4£©ĄūÓĆMg(OH)2Óėŗ¬SO2ŗĶO2µÄŃĢĘų·“Ӧɜ³ÉMgSO4ŗĶĮķŅ»ÖÖĪŽĪŪČ¾µÄ»ÆŗĻĪļ£¬æÉŅŌŹ¹ŃĢĘųĶŃĮņ£¬ĒėĪŹĮķŅ»ÖÖ²śĪļµÄ»ÆѧŹ½ĪŖ___”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com