(2006?绵阳)(1)市售塑料袋有的是用聚乙烯[(CH
2CH
2)
n]制成,有的是用聚氯乙烯[(CH
2CHCl)
n]制成,通过查阅资料可知:
(CH
2CHCl)
n+
O
2 2nCO
2+nH
2O+nHCl
其中n是上千或上万的数值;HCl气体极易溶于水,有刺鼻气味,其水溶液即是盐酸;鉴别盐酸的方法是加入AgNO
3溶液,观察是否产生白色沉淀.
①通过点燃的方法可以鉴别聚乙烯和聚氯乙烯.如果塑料袋点燃时有强烈的刺鼻气味,这种塑料袋可能是由
聚氯乙烯
聚氯乙烯
制成的.
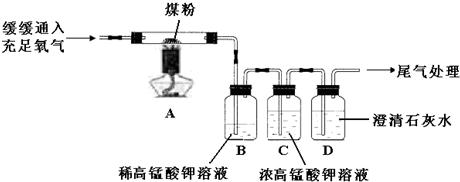
②某同学设计了如下图所示实验来探究塑料燃烧的产物.

若A瓶燃烧的是聚氯乙烯塑料,在B瓶中可以看到的现象是
试纸变红,瓶内壁有水雾
试纸变红,瓶内壁有水雾
,C、D两瓶中发出反应的化学方程式为
HCl+AgNO3═AgCl↓+HNO3、CO2+Ca(OH)2═CaCO3↓+H2O
HCl+AgNO3═AgCl↓+HNO3、CO2+Ca(OH)2═CaCO3↓+H2O
.若A瓶中用的是聚乙烯塑料,则在C瓶中能观察到的现象是
溶液中有气泡冒出
溶液中有气泡冒出
.
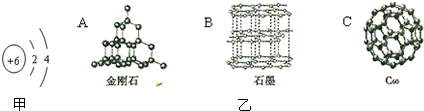
(2)(10分,除第④小题2分外,其余每空1分)在装潢、装饰和书写对联时,常用到一种“金粉”,已知这种“金粉”是由两种金属形成的合金粉末.三位同学做了如下探究实验.
甲同学:取少量“金粉”放入燃烧匙中,用酒精灯加热,发现“金粉”变黑,立即将燃烧匙伸入盛有H
2的集气瓶中,黑色粉末又恢复金黄色.
乙同学:取少量“金粉”放入试管中,加入足量稀盐酸,有气体产生,始终有红色固体不能溶解.
丙同学:通过定量实验测得一些数据,再计算出“金粉”中与稀盐酸反应的金属的相对原子质量为65.4.
综合分析上述实验结果回答下列问题:
①写出与实验现象对应的化学反应方程式,并判断反应类型.
甲同学的实验中金粉变黑:
,
化合
化合
反应
乙同学的实验中产生气体:
Zn+2HCl═ZnCl2+H2↑
Zn+2HCl═ZnCl2+H2↑
,
置换
置换
反应
②假设“金粉”是纯的黄金,在甲、乙两同学的实验中应观察到:甲
“金粉”始终不变色
“金粉”始终不变色
,乙
加盐酸时无现象
加盐酸时无现象
.
③在乙同学的实验中,若把稀盐酸换为AgNO
3溶液,可能发生反应的化学方程式为
Zn+2AgNO3═Zn(NO3)2+2Ag
Zn+2AgNO3═Zn(NO3)2+2Ag
、
Cu+2AgNO3═Cu(NO3)2+2Ag
Cu+2AgNO3═Cu(NO3)2+2Ag
.
④丙同学的实验中,至少应该测量的一组数据是
ABC或ABD
ABC或ABD
(填下列选项的字母标号).
A.“金粉”的质量 B.“金粉”溶于盐酸后剩余固体的质量
C.反应放出气体的质量 D.反应放出气体的体积和密度.



 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案

 ”和“
”和“ ”分别表示氢和氧两种元素的原子.
”分别表示氢和氧两种元素的原子.


