酒精灯 长颈漏斗 2KClO
3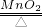
2KCl+3O
2↑ D 黑色的物质变为红色,在管口有水珠生成 CuCl
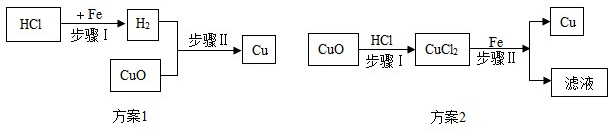
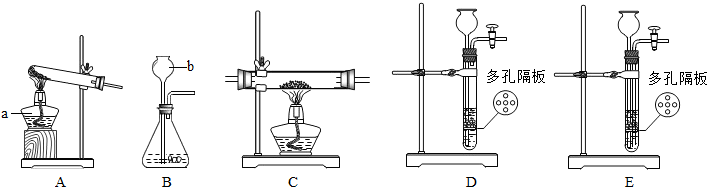
2+Fe═Cu+FeCl
2 BC或DC
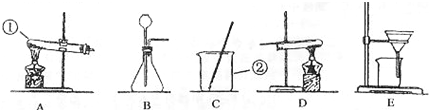
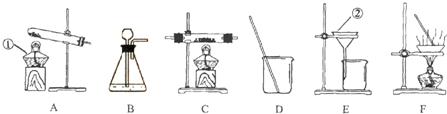
分析:①直接写出仪器的名称;
②氯酸钾分解产生了氯化钾和氧气,可以据此写出化学方程式;
③启普发生器能够控制反应的开始和停止,可以据此分析所给的仪器的特点来进行判断;
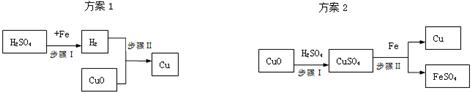
④Ⅰ、氧化铜为黑色固体,氢气具有还原性,可以和黑色氧化铜反应,可以据此解答该题;
Ⅱ、铁的活动性比铜强,所以可以将铜从氯化铜中置换出来,可以据此解答;
Ⅲ、方案1中铁与盐酸反应生成了氯化亚铁和氢气,而氢气还原氧化铜需要加热,可以据此选择装置.
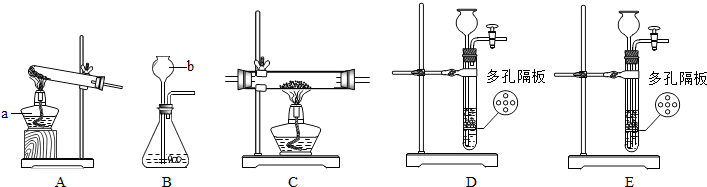
解答:①图中仪器a为酒精灯,b为长颈漏斗;
②氯酸钾与二氧化锰混合加热制氧气,同时还生成了氯化钾,其反应的化学方程式为:2KClO
3
2KCl+3O
2↑;
③分析图中的仪器可以知道,D和E都能控制反应,但是E中的导气管伸入的太长,生成的气体不易逸出,故D装置更类似于启普发生器;
④Ⅰ、方案1中的步骤Ⅱ反应为氢气还原氧化铜的反应,其现象为黑色的物质变为红色,在管口有水珠生成;
Ⅱ、方案2制取铜,写出步骤Ⅱ发生反应的化学方程式为:CuCl
2+Fe═Cu+FeCl
2;
Ⅲ、方案1中的步骤Ⅰ为铁和盐酸的反应,属于固液常温型反应,可以选用B或D装置,而步骤Ⅱ为氢气还原氧化铜的反应,该反应需要加热,应该选择C装置,故所需装置为BC或DC.
故答案为:①酒精灯;长颈漏斗;
②2KClO
3
2KCl+3O
2↑;
③D;
④Ⅰ、黑色的物质变为红色,在管口有水珠生成;
Ⅱ、CuCl
2+Fe═Cu+FeCl
2;
Ⅲ、BC或DC.
点评:本题主要考查实验装置的选取,化学方程式的书写,反应中的现象.属于综合性较强的题目,需要同学们细心才能做对.

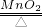 2KCl+3O2↑ D 黑色的物质变为红色,在管口有水珠生成 CuCl2+Fe═Cu+FeCl2 BC或DC
2KCl+3O2↑ D 黑色的物质变为红色,在管口有水珠生成 CuCl2+Fe═Cu+FeCl2 BC或DC 2KCl+3O2↑;
2KCl+3O2↑; 2KCl+3O2↑;
2KCl+3O2↑;