
 如图所示的是电解水实验装置.通电一段时间后,在两个试管中分别收集到气体a和气体b.请回答:
如图所示的是电解水实验装置.通电一段时间后,在两个试管中分别收集到气体a和气体b.请回答:分析 根据电解水产生的氢气体积大,氧气体积小,正极产生氧气,负极产生氢气,电解水获得的实验结论,要记住.然后根据化学方程式进行计算.普通的水的导电性较弱,加入硫酸钠或氢氧化钠是为了增强水的导电性.
解答 解:(1)气体a体积较大,是氢气,具有可燃性,若氢气不纯点燃易发生爆炸,所以点燃前要先检验其纯度;故填:氢气,验纯;
(2)气体b体积较小,是氧气,具有助燃性,可使带火星的木条复燃,电解水的化学方程式为:2H2O$\frac{\underline{\;点燃\;}}{\;}$2H2↑+O2↑
4 32
则生成氢气与氧气的质量比为:4:32=1:8;故填:带火星的木条,1:8;
(3)少量硫酸钠或氢氧化钠溶液具有良好的导电性,而纯水导电性很弱,反应较慢,在水中加入少量硫酸钠或氢氧化钠是为了增强水的导电性.
故填:增强水的导电性.
点评 本题难度不大,掌握电解水的实验现象、结论等是正确解答本题的关键.


 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案科目:初中化学 来源: 题型:选择题
| A. | 铁在氧气中燃烧:4Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 | |
| B. | 澄清石灰水和盐酸发生中和反应:CaO+2HCl=CaCl2+H2O | |
| C. | 检验混合气体中是否含有二氧化碳:CO2+2NaOH=Na2CO3+H2O | |
| D. | 用碳酸氢钠治疗胃酸过多:NaHCO3+HCl=NaCl+H2O+CO2↑ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | A | B | C | D |
| 实验 目的 | 清洗铁制品 表面的铁锈 | 除去氢氧化钠中 的碳酸钠 | 鉴别氯化钠 溶液和稀盐酸 | 检验一氧化碳中 混有二氧化碳气体 |
| 方案1 | 加适量稀盐酸 | 加水溶解 | 加锌粒 | 点燃 |
| 方案2 | 用水洗涤 | 加稀盐酸 | 加石蕊溶液 | 通入澄清石灰水 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
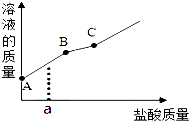 敞口放置的氢氧化钠溶液易吸收空气中的二氧化碳而变质.现向一定质量且部分变质的氢氧化钠溶液中逐滴加入稀盐酸,并振荡.如图表示反应过程中溶液质量随加入盐酸质量的变化而变化的情况.
敞口放置的氢氧化钠溶液易吸收空气中的二氧化碳而变质.现向一定质量且部分变质的氢氧化钠溶液中逐滴加入稀盐酸,并振荡.如图表示反应过程中溶液质量随加入盐酸质量的变化而变化的情况.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
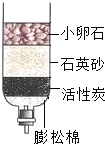 学校、家庭、办公室常用净水器的基本原理可用如图所示的简易净水装置表示.其中所用的小卵石、石英砂等的作用是( )
学校、家庭、办公室常用净水器的基本原理可用如图所示的简易净水装置表示.其中所用的小卵石、石英砂等的作用是( )| A. | 沉淀 | B. | 过滤 | C. | 吸附 | D. | 蒸馏 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 由碳、氢、氧三种元素组成 | |
| B. | 相对分子质量为46 | |
| C. | 一个二甲醚分子中含有9个原子 | |
| D. | 碳、氢、氧三种元素的质量比为2:6:1 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
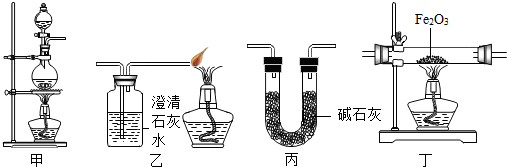
| 加热方式 | 通CO加热时间/min | 澄清石灰水变 浑浊时间/min | 产物颜色 | 产物能否全部 被磁铁吸引 |
| 酒精灯 | 30 | 5 | 黑色 | 能 |
| 酒精喷灯 | 30 | 1 | 黑色 | 能 |
| 样品序号 | 加热方式 | 元素组成和质量分数 |
| 产物样品Ⅰ | 酒精灯 | w(Fe)=74.4%、w(O)=25.6% |
| 产物样品Ⅱ | 酒精喷灯 | w(Fe)=100% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com