
 为测定某市售CaCO3药品中CaCO3的质量分数(杂质为SiO2,与稀HCl不反应),某同学的方法是:将样品与稀盐酸反应,测定反应后生成的CO2质量,再根据CO2的质量求出样品中CaCO3的质量,从而计算出样品中CaCO3的质量分数.为测定生成CO2的质量,他设计了如图的实验方案(已知;无水氯化钙是常见的干燥剂):
为测定某市售CaCO3药品中CaCO3的质量分数(杂质为SiO2,与稀HCl不反应),某同学的方法是:将样品与稀盐酸反应,测定反应后生成的CO2质量,再根据CO2的质量求出样品中CaCO3的质量,从而计算出样品中CaCO3的质量分数.为测定生成CO2的质量,他设计了如图的实验方案(已知;无水氯化钙是常见的干燥剂):分析 碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,反应前后的质量差即为反应生成二氧化碳的质量,根据二氧化碳质量可以计算碳酸钙的质量,进一步可以计算该方案测得样品中CaCO3的质量分数.
解答 解:①设碳酸钙质量为x,
样品质量为:574.57g-564.57g=10g,
反应生成二氧化碳质量为:574.57g-570.57g=4g,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 44
x 4g
$\frac{100}{x}$=$\frac{44}{4g}$,
x=9.09g,
该方案测得样品中CaCO3的质量分数是:$\frac{9.09g}{10g}$×100%=90.9%,
答:该方案测得样品中CaCO3的质量分数是90.9%.
②该实验中用稀HCl与CaCO3样品反应,而不用浓HCl与CaCO3样品反应,其原因是浓盐酸具有挥发性,会导致测量误差;
实验中无水氯化钙的作用是吸收二氧化碳气体中的水蒸气;
若实验中不用无水氯化钙,则测得的二氧化碳质量偏大,从而导致样品中CaCO3的质量分数与上述实验计算结果相比偏大.
故填:浓盐酸具有挥发性,会导致测量误差;吸收二氧化碳气体中的水蒸气;偏大.
点评 差量法在计算中的应用很广泛,解答的关键是要分析出物质的质量差与要求的未知数之间的关系,再根据具体的数据求解.


科目:初中化学 来源: 题型:多选题
| A. | 非金属元素在化合物里总是显负价 | |
| B. | 在H2中,H元素为零价 | |
| C. | 一种元素在同一化合物里可能有不同的化合价 | |
| D. | 在化合物中,正负化合价代数和不一定为零 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
| 反应前 | 反应后 | ||
| 实验数据 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物的质量 |
| 153.4克 | 10g | 160.1g | |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 11:18 | B. | 22:9 | C. | 11:37 | D. | 1:1 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
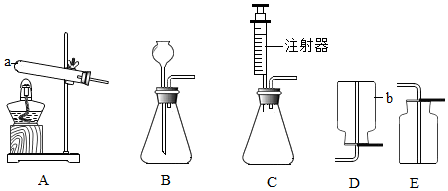
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com