
乙炔( )是生产聚氯乙烯的重要原料。用电石(主要成分为
)是生产聚氯乙烯的重要原料。用电石(主要成分为 )与水反应可制取乙炔,最终还可得到电石渣。某电石渣中含氢氧化钙
)与水反应可制取乙炔,最终还可得到电石渣。某电石渣中含氢氧化钙 ,其余为杂质,此电石渣可用于处理电镀厂排出的酸性废水。
,其余为杂质,此电石渣可用于处理电镀厂排出的酸性废水。
(1)乙炔中碳、氢元素的质量比为 。
(2)100kg上述电石渣中氢氧化钙的质量为 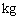 。
。
(3)用上述电石渣处理含硫酸 的酸性废水(假设电石渣中的杂质、废水中其他成分均不参加反应),求至少需要电石渣的质量(写出计算过程及结果)。
的酸性废水(假设电石渣中的杂质、废水中其他成分均不参加反应),求至少需要电石渣的质量(写出计算过程及结果)。
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:初中化学 来源: 题型:
21世纪的能源金属﹣锂(Li)
金属锂,被誉“21世纪的能源金属”,当前手机中广泛使用的电池,主要是高能锂电池.请回答下列问题:
(1)锂原子的原子结构示意图如图所示;锂原子在化学反应中容易 (填“得到”或“失去”)电子变成离子,其离子符号为 .
(2)研究表明,锂的金属活动性比较活泼.写出金属锂与稀硫酸反应的化学方程式 .
(3)金属锂除了制造锂电池外,还可以用于储存氢气,其原理是金属锂与氢气化合生成白色粉末状的氢化锂(LiH),氢化锂与水反应生成氢氧化锂和氢气.写出上述过程中发生反应的化学方程式 .

查看答案和解析>>
科目:初中化学 来源: 题型:
马英同学取某地石灰石样品12g进行测定实验,现将100g稀盐酸分五次加入石灰石样品中(杂质不溶于水也不参与反应),充分反应后测得生成气体的总质量如下表所示:
| 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
| 加入稀盐酸的质量/g | 20 | 20 | 20 | 20 | 20 |
| 生成气体的总质量/g | 1.1 | 2.2 | m | 4.4 | 4.4 |
试求:
(1)m的值为 g(1分)
(2)12g石灰石样品中碳酸钙的质量等于 g(2分)
(3)反应完全后最终溶液中氯化钙的质量分数? (3分)
(写出计算过程,计算结果精确至0.1)
查看答案和解析>>
科目:初中化学 来源: 题型:
 胃酸主要成分是盐酸,正常人胃液每日需要盐酸溶质质量约为6.5g~7.3g。某患者每日分泌盐酸溶质质量为9.0g,为治疗胃酸过多需服用图9所示抑酸剂,发生反应:Mg(OH)2+2HCl=MgCl2+2H2O。请计算并回答:按说明书用法用量,每天最多可中和胃液中盐酸溶质质量是多少克?理论上能否使该患者胃液中盐酸溶质质量恢复到正常范围?(写出计算过程,结果精确到0.001)
胃酸主要成分是盐酸,正常人胃液每日需要盐酸溶质质量约为6.5g~7.3g。某患者每日分泌盐酸溶质质量为9.0g,为治疗胃酸过多需服用图9所示抑酸剂,发生反应:Mg(OH)2+2HCl=MgCl2+2H2O。请计算并回答:按说明书用法用量,每天最多可中和胃液中盐酸溶质质量是多少克?理论上能否使该患者胃液中盐酸溶质质量恢复到正常范围?(写出计算过程,结果精确到0.001)
查看答案和解析>>
科目:初中化学 来源: 题型:
为了测定某含杂质7%的黄铜样品中铜的质量分数(杂质中不含铜、锌元素,杂质不溶于水,不与其它物质反应,受热也不分解),某化学小组进行了如下实验:
 (1)配制上述质量分数为14.6%的稀盐酸,需要质量分数为36.5%的浓盐酸的质量是______;
(1)配制上述质量分数为14.6%的稀盐酸,需要质量分数为36.5%的浓盐酸的质量是______;
(2)发生反应的化学方程式为____________________________________________;
(3)根据已知条件列出求解100g该黄铜样品中锌的质量(x)的比例式为__________;
(4)该黄铜样品中铜的质量分数是__________;
(5)向过滤后所得滤液中加入87.4g水,则最终所得溶液中溶质的质量分数是__________;
(6)欲将黄铜样品中的铜转化为铜盐,可将过滤后所得的不溶性物质洗涤、烘干,然后在空气中加热,充分反应,则可得到含杂质的氧化铜的质量是__________,再经过某些反应及操作就得到了所需铜盐。
查看答案和解析>>
科目:初中化学 来源: 题型:
已知X是有毒且不溶于水的气体,Y是不支持燃烧的气体,Z是不溶于水的固体,X、Y、Z之间有如下转化关系。请回答下列问题。

(1)写出X的化学式___________________________________________;
(2)写出Z和稀盐酸反应生成Y的化学方程式:___________________________
(3)“物质的组成与结构决定物质的性质”是重要的化学思想。气体X、Y都含有________元素和________元素,但它们的物理性质、化学性质都不同。请举出X、Y性质不同的一个例子________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com