
| A. | 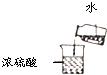 稀释浓硫酸 | B. |  称量氢氧化钠固体 | ||
| C. |  闻气体气味 | D. |  取用碳酸钠粉末 |
分析 A、浓硫酸的稀释,应把浓硫酸沿烧杯壁慢慢倒入水里,并用玻璃棒不断搅拌,防止液体溅出;
B、氢氧化钠能吸收空气中的水而潮解且有较强的腐蚀性,因此在称取所氧化钠时一定要放在玻璃容器内称取;
C、闻药品的味道,因许多药品有毒或有强烈的刺激性,在闻气味时应用手在瓶口轻轻扇动,使少量气体飘入鼻孔;
D、取用粉末状药品,试管横放用药匙把药品送到试管底部,然后试管慢慢竖起使药品缓缓滑入试管底部.
解答 解:A、图示中明确表明操作中是把水倒入浓硫酸里,这样会引起液体四溅,是错误操作,故不选;
B、图示中称取氢氧化钠时放在纸上进行称取,托盘会被腐蚀,错误操作,故不选;
C、图示把药品直接放在鼻子近处闻气味,若药品有毒或有强烈刺激性,这样做的后果将很可怕.错误操作,故不选;
D、图示的取用粉末状药品碳酸钠是正确操作,故选;
故选D.
点评 准确读取图中的信息,为正确作答的基础;掌握基本操作要领是解答的关键.


 英才计划期末调研系列答案
英才计划期末调研系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 某兴趣小组对鸡蛋壳的主要成分和含量进行了探究.
某兴趣小组对鸡蛋壳的主要成分和含量进行了探究.| 稀盐酸的用量 | 剩余固体的质量 |
| 第一次加入5.00g | 1.50g |
| 第二次加入5.00g | 1.00g |
| 第三次加入5.00g | 0.50g |
| 第四次加入5.00g | 0.30g |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 步骤 | 实验操作 | 预期现象与结论 |
| 1 | 各取2mL反应后的混合溶液分别加入A、B两只试管 | |
| 2 | 向A试管中滴加足量的稀硫酸,随即滴入几滴红色品红溶液 | 证明含有K2SO3 |
| 3 | 向B试管中,加入足量的氯化钡溶液,再加入足量的稀盐酸 | 先有白色沉淀,后有气体产生,沉淀部分溶解,证明含有K2SO4,则猜想3成立 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com