

分析 (1)通常情况下,锌和稀硫酸反应生成硫酸锌和氢气,氢气难溶于水,密度比空气小;
浓硫酸具有吸水性,可以用来干燥氢气、氧气、二氧化碳等气体;
显酸性的溶液不能使酚酞试液变色;
稀硫酸、硫酸锌都能够和氯化钡反应生成白色沉淀硫酸钡;
碳酸钠和稀硫酸反应生成硫酸钠、水和二氧化碳;
(2)氧化铜是黑色粉末,铜是红色固体;
根据提供的数据可以计算相关方面的问题;
氢氧化钠溶液能够吸收二氧化碳气体.
解答 解:(1)①在实验室制备并收集一瓶纯净干燥的氢气,所选装置的连接顺序为A→C→F,通过A装置制取氢气,通过C装置干燥氢气,通过F装置收集氢气;
②制备氢气发生反应的化学方程式为:Zn+H2SO4=ZnSO4+H2↑;
③加入酚酞试液时,无论溶液中是否含有稀硫酸,酚酞试液都不变色,因此不能用酚酞试液检验;
加入氯化钡溶液时,无论溶液中是否含有稀硫酸,都产生白色沉淀,因此不能用氯化钡溶液检验;
加入碳酸钠溶液时,如果有稀硫酸,则产生气泡,如果无稀硫酸,则不产生气泡,因此可以用碳酸钠溶液检验.
故填:A→C→F;Zn+H2SO4=ZnSO4+H2↑;选用Na2CO3溶液,向剩余废液中加入碳酸钠溶液,若存在硫酸,就会观察到产生气泡.
(2)①实验时,观察到装置B中的现象为黑色粉末逐渐变红色;
②若装置中不连接C1,通过测定装置B反应前后的质量变化计算出样品中CuO的纯度,因为水蒸气不影响对装置B反应前后的质量变化的计算,因此与实际值比较将不受影响;
③设与氢气反应的氧化铜质量为x,与一氧化碳反应的氧化铜质量为y,
反应后测定装置C2增加了1.8g,说明生成了1.8g水,装置D增加了2.2g,说明生成了2.2g二氧化碳,
CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O,CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2,
80 18 80 44
x 1.8g y 2.2g
$\frac{80}{x}$=$\frac{18}{1.8g}$,$\frac{80}{y}$=$\frac{44}{2.2g}$,
x=8.0g,y=4.0g,
则该样品中CuO的纯度为:$\frac{8.0g+4.0g}{16g}$×100%=75.0%;
④评价:反应前后装置D的增重将因水煤气混有CO2而偏大,导致计算出的CuO纯度偏大;
建议:应在气体进入装置B前,将水煤气中的CO2和水蒸气都除净,正确的实验方案设计为:
水煤气→D1→C1→B→C2→D2→H.
故填:黑色粉末逐渐变红色;不受影响;75.0%;
评价:反应前后装置D的增重将因水煤气混有CO2而偏大,导致计算出的CuO纯度偏大;
建议:应在气体进入装置B前,将水煤气中的CO2和水蒸气都除净,正确的实验方案设计为:水煤气→D1→C1→B→C2→D2→H.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

| 实验步骤 | 设计这一步骤的目的 | 实验现象 | 实验结论 |
| ①将NaOH溶液加热煮沸 | ①除去溶液中的氧气 | 溶液变红,过一会儿红色消失 | 甲同学猜想不正确(填“正确”或不正确”) |
| ②向冷却后的溶液中滴人酚酞,并滴一些植物油在其上方 | ②隔绝氧气 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
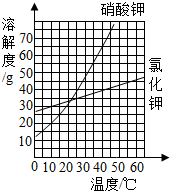 如图是氯化钾和硝酸钾两种固体溶解度曲线图.
如图是氯化钾和硝酸钾两种固体溶解度曲线图.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 请回答以下问题.
请回答以下问题.查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Ba2+、Cu2+、SO42- | B. | Na+、OH-、Cl- | C. | K+、Cl-、MnO4- | D. | H+、Ca2+、CO32- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com