
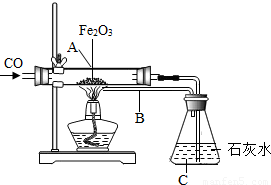
 有位同学设计了一氧化碳与氧化铁反应的实验,装置及所用药品如图所示,请回答下列问题.
有位同学设计了一氧化碳与氧化铁反应的实验,装置及所用药品如图所示,请回答下列问题. 2Fe+3CO2求出一氧化碳的质量;
2Fe+3CO2求出一氧化碳的质量; 2Fe+3CO2
2Fe+3CO2


科目:初中化学 来源: 题型:阅读理解
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 方 案 | 现 象 和 结 论 |
| 步骤1:取少量白色固体C于烧杯中,加入适量的水充分搅拌后,得到浑浊液体,滴入 酚酞试液 酚酞试液 溶液. |
溶液变成红色. |
| 步骤2:将步骤1的浑浊液过滤,滤渣置于试管中,滴入足量的 盐酸 盐酸 溶液. |
现象是 产生气泡 产生气泡 .猜想成立.此步发生反应的化学方程式是 CaCO3+2HCl=CaCl2+H2O+CO2↑ CaCO3+2HCl=CaCl2+H2O+CO2↑ . |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 碱石灰总质量 | 浓硫酸总质量 | |
| 反应前 | 356.8g | 156.6g |
| 反应后 | 359.0g | 158.4g |
查看答案和解析>>
科目:初中化学 来源:2013年山东省青岛市中考化学模拟试卷(五)(解析版) 题型:填空题
| 碱石灰总质量 | 浓硫酸总质量 | |
| 反应前 | 356.8g | 156.6g |
| 反应后 | 359.0g | 158.4g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com