
硫酸和盐酸既是实验室常用的试剂,也是重要的化工原料。写出用稀硫酸除去铁锈的化学方程式: ; 打开盛有浓盐酸和浓硫酸试剂瓶的瓶盖,立即就能把它们区分开来,这是因为: ;将20g质量分数为98%的浓硫酸稀释为10%的硫酸,需要水的质量为 g。
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案科目:初中化学 来源: 题型:填空题
请从下列物质中选择填空(填序号)
| A.氮气 | B.酒精 | C.生石灰 | D.铜 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
(4分)请用线段连接有对应关系的相邻两列间的点。
物质的化学式 物质的用途
熟石灰● ● 包装食品
氯化钠 ● ● 改良酸性土壤,配制波尔多液
漂白粉 ● ● 生产氯气、烧碱,做调味品
聚乙烯 ● ● 饮用水消毒
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
(4 分)建国 60 多年来,我国化学基础科学的发展,取得了举世瞩目的成就。我国科学家用滤纸和二氧化钛(TiO2)薄膜制作出一种新型“纳米纸”,又在纳米纸上“铺”一层“萘胺”(C10H9N)染料,制成一种试纸,用于检测食品中亚硝酸盐浓度的高低。
(1)二氧化钛中 Ti 的化合价为 。
(2)萘胺的一个分子中,C、H、N 三种原子的个数之比为 (填最简整数比)。
(3)已知 NaNO2 能发生如下反应(化学方程式已配平):
2NaNO2+2KI+2H2SO4=I2+2M↑+2H2O+Na2SO4+K2SO4,则 M 的化学式是 。
(4)根据上述反应,可用化学试纸及生活中常见物质进行实验来鉴别亚硝酸盐和食盐,现有碘化钾淀粉试纸,则还需选用下列生活中的常见物质为________(填序号)。
①食用油 ②白酒 ③食醋 ④牛奶
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
将V1mL3.65% HCl溶液逐滴滴入盛有V2mL未知浓度的
NaOH溶液的烧杯中(图1),测量并记录溶液的pH变化(图2)和
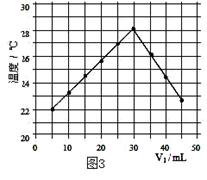
温度变化(图3)。(实验中始终保持 V1+V2=50.0mL且各种溶液密度
均为1.0g/mL)。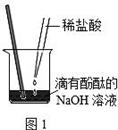
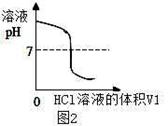
(1)图2中V1="0" mL时,图1中烧杯内溶液的颜色显 色;
(2)实验中发生反应的化学方程式为 ;
(3)图2中的pH=7时,此时滴入的HCl溶液的体积V1= mL;
(4)通过该实验给出的判断,其中正确的是 ;
| A.进行该实验时环境温度为22℃ |
| B.该实验表明化学能可转化为热能 |
| C.该实验表明有水生成的反应都是放热反应 |
| D.溶液由碱性转变为中性,再转变为酸性且酸性不断减弱 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
(5分)请根据下列表述回答问题:
(1)已知A、B、C、D均含有两种元素。固体A中加入液体B,能放出大量热。固体C中加入液体D,有气泡产生,充分反应后过滤,只得到液体B和固体C。
①A跟B反应的生成物可用于改良酸性土壤或用于建筑材料等,则A的化学式为________。
②C跟D发生反应的化学方程式为________。
(2)固体E、F和液体G、H四种物质中,任意一种固体与任意一种液体混合均有气泡产生。E通过其它反应能生成F。
①若E为单质,E、F的化学式可能为 (写一组即可)。
②若E和F均含三种元素,E生成F的化学方程式为 。固体E和二氧化硅在高温条件下可生成硅酸钠(Na2SiO3)和一种能产生温室效应的常见气体,该反应的化学方程式为: 。
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
氨气(NH3)是一种无色有刺激性气味的气体,极易溶于水,它的水溶液称为氨水,显碱性。氨气在化学工业中用途很广泛,例如制化肥、制纯碱等。近年来,氨气还用于环境治理。
(1)“候氏制碱法”的两步主要反应原理可表示为:
①NH3+CO2 +H2O+NaCl=NaHCO3↓+NH4Cl,
②2NaHCO3 Na2CO3+ H2O + CO2↑。其中,NaHCO3属于 (“酸”、“碱”或“盐”),反应②属于 反应,Na2CO3的俗名叫 。
Na2CO3+ H2O + CO2↑。其中,NaHCO3属于 (“酸”、“碱”或“盐”),反应②属于 反应,Na2CO3的俗名叫 。
(2)在细菌作用下,用氨处理含甲醇的工业废水,使其变为无毒的N2和CO2,从而清除对环境的污染,有关的反应为:6NH3 + 5CH3OH + 12B = 3N2↑+ 5CO2↑+ 19H2O,其中B物质的化学式是 。
(3)氨气可以被硫酸吸收,生成可以用作氮肥的硫酸铵,该反应的化学方程式为:2NH3+H2SO4 = (NH4)2SO4。若用盐酸吸收氨气,则反应的化学方程式为: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com