
科目:初中化学 来源: 题型:阅读理解
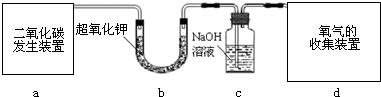
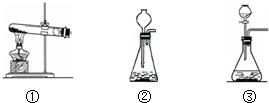
| 实验步骤 | 实验现象 | 实验结论 |
| 将二氧化碳与超氧化钾反应后的固体 | 猜想 (填序号)是正确的,二氧化碳与超氧化钾反应生成的化合物是(填名称 ). |
查看答案和解析>>
科目:初中化学 来源: 题型:
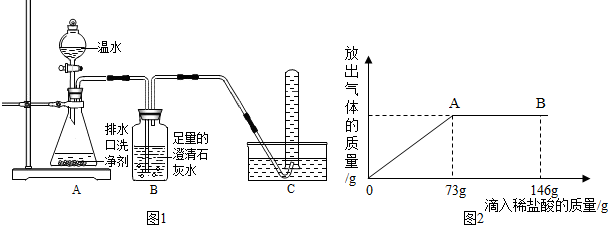
 24、某化学兴趣活动小组的同学学习“灭火器原理”后,设计了如下图所示实验,并对反应后锥形瓶中残留废液进行探究.
24、某化学兴趣活动小组的同学学习“灭火器原理”后,设计了如下图所示实验,并对反应后锥形瓶中残留废液进行探究.查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 实验操作 | 主要实验现象 | 结论 |
| ①取样,滴加 CaCl2 CaCl2 溶液 |
出现白色沉淀 出现白色沉淀 |
证明溶液中有Na2CO3 |
| ②取上层清液,滴加 Ca(OH)2 Ca(OH)2 溶液 |
无白色沉淀产生 | 证明溶液中无NaHCO3 |
| ③取样, 加入过量氯化钙溶液,充分反应后滴加酚酞试剂 加入过量氯化钙溶液,充分反应后滴加酚酞试剂 |
不变色 不变色 |
证明溶液中无NaOH |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 正确或错误 | 理 由 | |
小健的方案 |
错误 错误 |
滴加稀盐酸,只能和碱性物质反应,但不能和钡离子结合成沉淀,消除钡离子的污染 滴加稀盐酸,只能和碱性物质反应,但不能和钡离子结合成沉淀,消除钡离子的污染 |
小康的方案 |
正确 正确 |
滴加稀硫酸,既除去了废液中的碱使溶液呈现中性,又使钡离子转化成了难溶性的硫酸钡沉淀,实现了绿色排放 滴加稀硫酸,既除去了废液中的碱使溶液呈现中性,又使钡离子转化成了难溶性的硫酸钡沉淀,实现了绿色排放 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
某校化学课外兴趣小组的小刚和小强同学到实验室去做探究实验时,他们意外发现实验桌上有一瓶敞口放置的氢氧化钠固体。根据所学化学知识,他们认为此瓶氢氧化钠固体变质了,接着他们对这瓶氢氧化钠固体变质情况进行了探究。
提出问题:氢氧化钠固体变质程度如何?
查阅资料:
(1)20℃部分物质的溶解性表
| OH- | NO3- | Cl- | SO42- | CO32- | |
| Na+ | 溶 | 溶 | 溶 | 溶 | 溶 |
| Ca2+ | 微 | 溶 | 溶 | 微 | 不 |
(2)氯化钙和氯化钠溶液呈中性,不能使无色酚酞变色
猜想与假设:
小刚猜想:氢氧化钠可能部分变质,生成了碳酸钠。
小强猜想: 。
实验探究:小刚和小强设计探究实验方案,证明了他们各自的猜想。探究过程如下:
| 实验步骤 | 实验操作 | 实验现象 | 实验结论或化学方程式 |
| 步 骤 一 | 取样品,加水配制成溶液,并向其中滴加适量氯化钙溶液,充分反应后过滤 | 有 生成 | 氢氧化钠已变质。写出加入氯化钙溶液后发生反应的化学方程式 。 |
| 步 骤 二 | 取上述少量滤液于试管中,滴加无色酚酞溶液 | 酚酞溶液变 为 色 | 氢氧化钠部分变质 |
得出结论:小刚的猜想正确。
表达与交流
(1)用化学方程式表示氢氧化钠变质的原因: 。
(2)在实验室里氢氧化钠需要密封保存。药品密封保存的原因很多,请你写出浓盐酸需要密封能够保存的原因 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com