
 实验室中浓硫酸的标签如图所示.请根据有关信息计算:
实验室中浓硫酸的标签如图所示.请根据有关信息计算:分析 (1)根据m=ρv,结合浓硫酸的商标图中的密度和体积进行分析解答.
(2)根据溶液稀释前后溶质的质量不变,结合题意进行分析解答.
(3)根据浓硫酸的稀释方法(酸入水,沿器壁,慢慢倒,不断搅)进行分析解答.
解答 解:(1)500mL=500cm3,m=ρv,该试剂瓶中硫酸溶液的质量是1.84g/cm3×500cm3=920g.
(2)设需这种浓硫酸的质量为x,根据溶液稀释前后,溶质的质量不变,
则100g×19.6%=x×98% x=20g.
(3)稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时地扩散;一定不能把水注入浓硫酸中.
故答案为:(1)920;(2)需这种浓硫酸20g;(3)将浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌.
点评 本题难度不大,掌握m=ρv、溶液稀释前后溶质的质量不变、浓硫酸的稀释方法是正确解答本题的关键.


 每课必练系列答案
每课必练系列答案 巧学巧练系列答案
巧学巧练系列答案科目:初中化学 来源:山东省临沂市蒙阴县2017届九年级第二轮模拟考试化学试卷 题型:选择题
关于“舌尖上的化学”,下列说法不科学的是( )
A.为了身体健康,必须均衡膳食
B.为预防缺碘性疾病,可食用适量海带
C.为了保质,用甲醛溶液泡制米粉
D.为使发面食品松软可口,制作时可添加适量碳酸氢钠
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
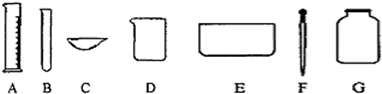
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 溶液中的OH-刚好与加入的H+完全结合 | |
| B. | 溶液的颜色刚好变为蓝色 | |
| C. | 溶液的颜色刚好变为无色 | |
| D. | 无法判断 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
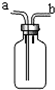 如图是化学中“著名”的多用途装置,有如下用途:
如图是化学中“著名”的多用途装置,有如下用途:查看答案和解析>>
科目:初中化学 来源: 题型:多选题
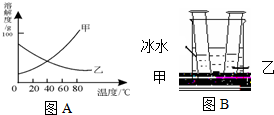
| A. | 乙溶液中溶质的质量分数增大 | B. | 装甲溶液的试管中固体增多 | ||
| C. | 试管里甲、乙物质的溶解度都增大 | D. | 两支试管里剩余的固体都增多 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 已知:常温下二氧化硫是无色气体,它能与水反应生成亚硫酸(SO2+H2O=H2SO3),亚硫酸的酸性比醋酸的酸性要强.为了验证SO2能与水发生反应,请你来共同研究.
已知:常温下二氧化硫是无色气体,它能与水反应生成亚硫酸(SO2+H2O=H2SO3),亚硫酸的酸性比醋酸的酸性要强.为了验证SO2能与水发生反应,请你来共同研究.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
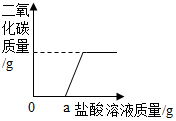 一瓶久置的氢氧化钠固体已经发生了变质.某研究性学习小组为了探究变质程度,作出如下猜想:可能部分变质,固体是NaOH和 Na2CO3的混合物;可能全部变质,固体是Na2CO3.
一瓶久置的氢氧化钠固体已经发生了变质.某研究性学习小组为了探究变质程度,作出如下猜想:可能部分变质,固体是NaOH和 Na2CO3的混合物;可能全部变质,固体是Na2CO3.| 样品质量 | 反应前总质量 | 反应后总质量 |
| 10.6克 | 148.5克 | 146.3克 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com