
【题目】氯酸钾在工业上用于制造焰火、漂白剂等,在实验室可用于制造氧气。工业上利用石灰浆制备氯酸钾的流程是:

(1)写出实验室用氯酸钾制取氧气的化学方程式____________________。
(2)在实验室里,“操作a”中需要用到玻璃棒,其作用是__________。
(3)“反应1”的化学反应方程式为:6Ca(OH)2+6Cl2=Ca(ClO3)2+5CaCl2+6X,Ca(ClO3)2的名称是__________,X的化学式为__________。
(4)下表是有关物质常温下的溶解度。
物质 | KCl | CaCl2 | KClO3 | Ca(ClO3)2 |
溶解度/g | 34.2 | 74.5 | 7.3 | 209.0 |
“反应2”为复分解反应,参看表中溶解度,写出该反应的化学方程式__________。
(5)上述石灰浆可由电石(CaC2)与水反应制得。现有某电石渣,其中含氢氧化钙92.5%,用该电石渣处理含硫酸49Kg的酸性废水(假设电石渣中的杂质、废水中其他成分均不参加反应),需要电石渣的质量是__________kg。
【答案】2KClO3![]() 2KCl+3O2↑ 引流 氯酸钙 H2O Ca(ClO3)2+2KCl=2KClO3↓+CaCl2 40
2KCl+3O2↑ 引流 氯酸钙 H2O Ca(ClO3)2+2KCl=2KClO3↓+CaCl2 40
【解析】
(1)实验室用氯酸钾制取氧气,是氯酸钾和二氧化锰在加热条件下生成氯化钾和氧气,对应的化学方程式为:2KClO3![]() 2KCl+3O2↑;
2KCl+3O2↑;
(2)在实验室里,“操作a”即为过滤,过滤中需要用到玻璃棒,其作用是引流;
(3)“反应1”的化学反应方程式为:6Ca(OH)2+6Cl2═Ca(ClO3)2+5CaCl2+6X,Ca(ClO3)2的中酸根为氯酸跟,所以化合物对应的名称是氯酸钙,反应中,反应前钙原子6个,氧原子12个,氢原子12个,氯原子12个,反应后现有钙原子6个,氧原子6个,氯原子12个,缺少12个氢原子和6个氧原子,这些微粒分布在6个X分子中,所以X的化学式为H2O;
(4)“反应2”为复分解反应,是氯酸钙和氯化钾反应,根据给出的溶解度可知,氯酸钾溶解度最小,所以生成物为氯酸钾和氯化钙,对应的化学方程式 Ca(ClO3)2+2KCl=2KClO3↓+CaCl2;
(5)设需要电石渣的质量是x,

![]()
x=40kg。


 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案科目:初中化学 来源: 题型:
【题目】酸、碱、盐在生产生活中具有广泛的用途。化学实验室中有失去标签的四瓶无色溶液:稀盐酸、氢氧化钙溶液、碳酸钠溶液、酚酞试液,现将其任意编号为A、B、C、D.然后两两组合进行实验,其中部分现象如下表,请回答:
实验 | A+B | A+C | B+C | B+D |
现象 | 溶液变红 | 溶液变红 | 产生沉淀 | 产生气体 |
(1)配酞试液是____________(填编号);
(2)B与C反应的化学方程式为____________________。
(3)写出D的一种用途:____________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】图1是新教材化学书的封面,该图片蕴含许多化学知识,试回答:
(1)图1中物质的变化是_______变化(填“物理”或“化学”)它反映出的环境问题是________,解决这种环境问题的方法是___________(答一点)。
(2)人类对物质的宏观和微观认识有图2关系,图中化学名词②是_______;若将(图2)中“物质”改成(图1)中的“液体”,并要求按照:
![]()
进行描述,则相应的语言应是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学小组同学在课外读物中看到:“加热时,过氧化钠(Na2O2)能与木炭发生化学反应”。他们决定探究Na2O2与木炭反应的产物。
(猜想与假设)木炭与Na2O2反应可能生成4种物质:CO、CO2、Na2O和Na2CO3。
(查阅资料)
① 碱性的碳酸钠溶液与中性的CaCl2溶液能发生复分解反应。
② 氧化钠(Na2O)是白色固体,与H2O反应生成NaOH。
③ 氯化钯(PdCl2)溶液能检验CO的存在,向溶液中通入CO,产生黑色沉淀。
(进行实验)同学们在老师的指导下设计了如下图所示装置(部分夹持仪器已略去)。
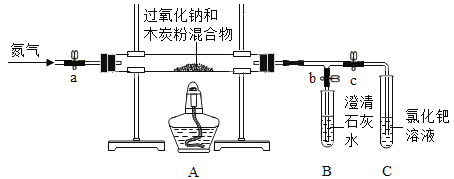
序号 | 实验操作 | 主要实验现象 | 实验结论 |
① | 检查装置气密性。向玻璃管中加入过氧化钠和过量木炭粉的混合物。打开弹簧夹a、b,关闭c,从装置左端通一段时间N2。 | A中无明显变化,B中有大量气泡冒出。 | 气密性良好。 |
② | 关闭a,点燃酒精灯。 | 试管中发生剧烈反应,产生火花,________________。 | 产物中没有CO2。 |
③ | 打开c,关闭b。 | C中PdCl2溶液没有明显变化。 | ___________________。 |
④ | 打开a,继续通N2,停止加热,待冷却后停止通N2。取出少量反应后固体于试管中,加入足量稀盐酸,迅速用带导管的橡胶塞塞紧试管口,导管另一端通入石灰水中。 | _____________________。 | 产物中有Na2CO3。 |
(解释与结论)
(1)检验第4种物质存在的实验方案:取出少量反应后固体于试管中,_______________,则第4种物质存在。
(2)Na2O2与木炭反应的化学方程式为_________________________________。
(反思与评价)实验操作④中若不通入N2,可能造成的结果是________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属材料在生产、生活中应用广泛。
(1)铝块能被加工成很薄的铝箔,是利用了铝的__________性。
(2)钢铁是使用最多的金属材料,钢的硬度比纯铁的硬度__________(填“大”或“小”)。
(3)自行车的支架是铁制品,为防止锈蚀,在其表面刷漆,其防锈原理是__________。
(4)用一定量AgNO4溶液进行下图所示实验。

①在固体A上滴加稀盐酸,没有气泡产生,则固体A的组成是__________。
②溶液B呈蓝色,溶液B中一定含有的金属阳离子是__________(写离子符号)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向53g质量分数为10%的碳酸钠溶液中逐滴加入质量分数为5%的稀盐酸,生成二氧化碳的质量随加入盐酸质量的变化关系如图所示.(不考虑CO2的溶解)

已知:
OB段反应的化学方程式为Na2CO3+HCl═NaCl+NaH CO3
BD段(不含B点)反应的化学方程式为NaH CO3+HCl═NaCl+H2O+CO2↑
请回答:
(1)53g质量分数为10%的碳酸钠溶液中溶质质量为___________g.
(2)A点对应溶液中溶质有_________(填化学式).
(3)B点横坐标为________(计算结果保留1位小数,下同)
(4)假设C点横坐标为54.75,计算C点对应的二氧化碳质量.(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列化学用语书写正确的是
A. 2 个氯原子:Cl2
B. 3 个一氧化氮分子:3NO
C. 5 个铁离子:5Fe2+
D. 氧化镁中镁元素的化合价为+2价:![]()
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人们的日常生活离不开金属,高科技新材料的开发和应用也需要金属.
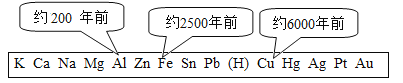
(1)上图表示金属活动性顺序中铝、铁和铜被人类大规模开发利用的大致年限,根据图中数据和相关化学知识,你认为金属大规模开发利用的先后顺序与下列因素无关_____
A 金属冶炼的难易程度
B 地壳中金属元素的含量
C 金属的活动性
(2)请用一个化学方程式说明铁的金属活动性比铜强_____.
(3)工业上电解氧化铝制取金属铝的化学方程式是:2Al2O3![]() 4Al+3O2↑,电解51t的氧化铝最多可生产多少吨铝?
4Al+3O2↑,电解51t的氧化铝最多可生产多少吨铝?
(4)实际生产中氧化铝可从铝土矿提炼获得.要生产相同质量的铝,所需铝土矿的质量应_(填“大于”、“小于”或“等于”)氧化铝质量_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在化学课上,甲同学将燃烧的钠迅速伸入到盛有CO2的集气瓶中,钠在其中继续燃烧,反应后冷却,瓶底附着黑色颗粒,瓶壁上粘附着白色物质。
(提出问题)黑色颗粒和白色物质是什么?
(进行猜想)甲认为黑色颗粒是________,白色物质可能是Na2O或________或________,乙同学还认为白色物质是氢氧化钠。
甲同学立刻认为乙同学的猜想是错误的,其理由是____________________________。
(查阅资料)氧化钠为白色粉末,溶于水生成氢氧化钠:Na2O+H2O===2NaOH
(实验探究)甲同学对白色物质进行实验探究。
实验方案 | 实验操作 | 实验现象 | 结论 |
方案1 | 取样品少量于试管中,加入适量水,振荡,样品全部溶于水,向其中加入无色醉酞试液 | 溶液变成红色 | 白色物质为Na2O |
方案2 | ①取样品少量于试管中,加入适量水,振荡,样品全部溶于水,向其中加入过量的CaCI2溶液 | 出现白色沉淀 | 白色物质是_____ |
②静置片刻,取上层清液于试管中,滴加无色酚酞试液 | 无明显现象 |
(反思评价)丙同学认为方案1得到的结论不正确,其理由是________________。
(得出结论)钠在二氧化碳中燃烧的化学方程式为___________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com