
分析 氯酸钾受热分解生成了氧气,所以固体质量变化是由于氧气的质量所致,所以可以求算氧气的质量,进而根据化学方程式计算氯酸钾的质量,最后确定二氧化锰的质量.
解答 解:
(1)氯酸钾(KClO3)中钾元素的质量分数(此处没有必要根据方程式计算,而是要根据化学式计算)=$\frac{39}{39+35.5+16×3}$×100%≈31.84%
(2)根据质量守恒定律可得生成的氧气的质量为30g-20.4g=9.6g
设生成9.6g氧气需要的氯酸钾的质量为x.
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
245 96
x 9.6g
$\frac{245}{96}$=$\frac{x}{9.6g}$
x=24.5g
则原混合物中二氧化锰的质量为30g-24.5g=5.5g.
答:(1)氯酸钾中钾元素的质量分数为31.84%;
(2)原混合物中二氧化锰的质量为5.5g.
点评 氯酸钾种钾元素的质量分数求算不要受题干影响,而是根据化学式计算.根据固体的质量变化求算氧气的质量,这是常见的质量差量法求算,建议平时多总结差量法的运用.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
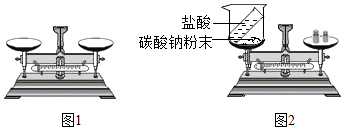 请根据题目要求回答下列问题.
请根据题目要求回答下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 生成2.0 gCO2气体 | B. | 原来CaCO3为12.5 g | ||
| C. | 生成了5.6 gCaO | D. | 剩余CaCO3为3.0 g |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验步骤及操作方法 | 预期的实验现象 | 实验结论 |
| ①取少量过氧化钙放入试管中,加足量的水,将带火星的小木条伸入试管中. | 木条复燃 | 有氧气生成 |
| ②向步骤1得到的溶液中通入CO2 | 溶液变浑浊 | 有氢氧化钙生成 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ②③ | B. | ①②③ | C. | ①②④ | D. | ①② |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com