
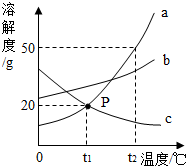
 如图所示是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点,据图回答:
如图所示是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点,据图回答:分析 根据题目信息和溶解度曲线可知:a、b两种固体物质的溶解度,都是随温度升高而增大,而c的溶解度随温度的升高而减少;在t2℃时,a、b、c三种物质的饱和溶液能通过降温使其变为不饱和溶液的是c,因为c的溶解度随温度的升高而减少;在t2℃时,将50ga物质加入50g水中充分搅拌溶解,所得溶液溶质质量分数=$\frac{50g}{150g}×100%≈33.3%$;t1℃时,用托盘天平称取15ga物质于一个烧杯中,再用100mL量筒量取75mL水加入烧杯中充分搅拌溶解即得a的饱和溶液,因为在该温度下a的溶解度是50g;若量取水时仰视读数,水实际量多了,则所得溶液为不饱和溶液;若称取a物质时a与砝码位置放反了(10g以下用游码),则所得溶液的质量分数=$\frac{5g}{5g+75g}×100%=6.25%$;在t2℃时,将a、b、c三种物质的不饱和溶液变为饱和溶液,都适用的方法有:增加溶质;蒸发溶剂;将t1℃时a、b、c三种物质饱和溶液的温度升高到t2℃时,三种溶液的溶质质量分数大小关系是:b>a>c,升温后,a、b的质量分数不变,c的质量分数减小.
解答 解:(1)在t2℃时,a、b、c三种物质的饱和溶液能通过降温使其变为不饱和溶液的是c,因为c的溶解度随温度的升高而减少;故答案为:c;
(2)在t2℃时,将50ga物质加入50g水中充分搅拌溶解,所得溶液溶质质量分数=$\frac{50g}{150g}×100%≈33.3%$;故答案为:33.3%;
(3)t1℃时,用托盘天平称取15ga物质于一个烧杯中,再用100mL量筒量取75mL水加入烧杯中充分搅拌溶解即得a的饱和溶液,因为在该温度下a的溶解度是50g;若量取水时仰视读数,水实际量多了,则所得溶液为不饱和溶液;若称取a物质时a与砝码位置放反了(10g以下用游码),则所得溶液的质量分数=$\frac{5g}{5g+75g}×100%=6.25%$;故答案为:100;75;不饱和;6.25%;
(4)在t2℃时,将a、b、c三种物质的不饱和溶液变为饱和溶液,都适用的方法有:增加溶质;蒸发溶剂;故答案为:增加溶质、蒸发溶剂;
(5)将t1℃时a、b、c三种物质饱和溶液的温度升高到t2℃时,三种溶液的溶质质量分数大小关系是:b>a>c,升温后,a、b的质量分数不变,c的质量分数减小;故答案为:C;
点评 本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液和溶质质量分数的计算,有关的计算要准确,本考点主要出现在选择题和填空题中.


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:初中化学 来源: 题型:选择题
| A. | 电视机着火时用水浇灭 | |
| B. | 进入久未开启的菜窖用手电筒照明 | |
| C. | 用钢丝刷擦洗铝锅上的污垢 | |
| D. | 厨房天然气泄漏,立即关闭阀门并轻轻开窗通风 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 如图是配制好的稀盐酸的标签,请根据标签上的文字信息,进行计算:
如图是配制好的稀盐酸的标签,请根据标签上的文字信息,进行计算:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 物质 | A | B | C | D |
| 肥皂水 | 食醋 | 牙膏 | 食盐水 | |
| pH | 10 | 3 | 9 | 7 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 南京第二届夏季青奥会上,中国代表团获得金银铜奖牌共计63枚.
南京第二届夏季青奥会上,中国代表团获得金银铜奖牌共计63枚.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
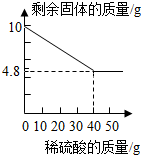
| 实验操作 | 实验现象 | 实验结论 |
| 取少量红色固体加入到足量稀硫酸溶液中 | 若无明显现象 | 假设1成立 |
| 若固体部分(选填“全部”或“部分”)溶解,溶液由无色变蓝色 | 假设2和假设3均成立 |
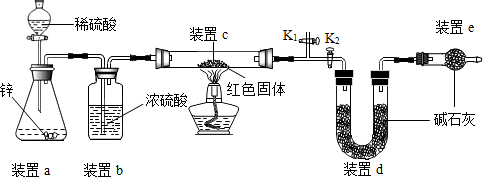
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用灼烧法鉴别羊毛和化纤 | |
| B. | 用肥皂水鉴别硬水和软水 | |
| C. | 加熟石灰粉末研磨,区分氯化铵和硫酸铵 | |
| D. | 用紫甘蓝和酒精溶液制酸碱指示剂 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
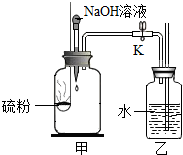 实验小组用右图所示装置进行实验.已知:2NaOH+SO2═Na2SO3+H2O
实验小组用右图所示装置进行实验.已知:2NaOH+SO2═Na2SO3+H2O| A. | 步骤①中,硫燃烧呈淡蓝色火焰,瓶内气压减小 | |
| B. | 步骤②中,甲装置内的气压减小,至与大气压相等 | |
| C. | 步骤③中,乙中的长导管口处冒气泡 | |
| D. | 步骤③中,甲装置内的气压增大,至与大气压相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com