
| A. | 电解水的基本反应类型是分解反应 | |
| B. | 混合物中一定含有两种或两种以上元素 | |
| C. | 催化剂在化学反应中能改变化学反应速率 | |
| D. | aL水和bL酒精混合后,总体积小于(a+b)L |
科目:初中化学 来源: 题型:实验探究题
| 判断 | 依据 |
| 不是KMnO4 | KMnO4能溶于水形成紫红色溶液 |
| 不是K2MnO4(填化学式) | 冲洗试管时出现深绿色溶液,说明该物质能溶于水 |
| 是MnO2 | 其他实验用过MnO2,知道它是不溶于水的黑色固体 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
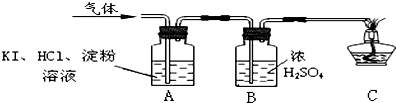
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
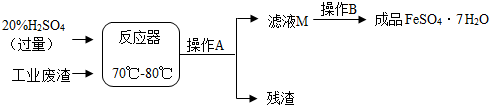
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
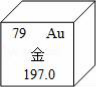 如图是金元素在元素周期表中的信息示意图.从图中获取的信息正确的是A.
如图是金元素在元素周期表中的信息示意图.从图中获取的信息正确的是A.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com