
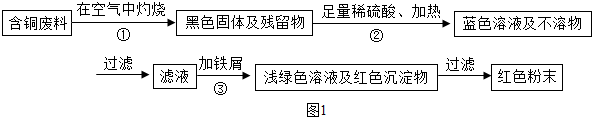
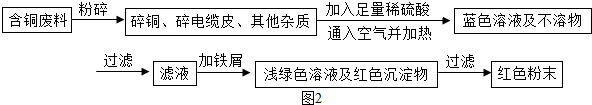
分析 解答本题关键是要知道置换铜必须用铁,因为还要得到硫酸亚铁,为了反应充足加入的试剂要过量,再利用铁能与硫酸反应,铜不能与硫酸反应将铜和铁分开.
解答 解:(1)铜在空气中灼烧生成黑色固体氧化铜,氧化铜与硫酸反应生成蓝色硫酸铜,与铁屑反应置换出铜,反应方程式为:CuO+H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+H2O; Fe+CuSO4═FeSO4+Cu;
(2)从环保角度对两套方案的不同部分进行比较,甲方案第一步灼烧会产生污染空气的气体,粉尘,烟雾,由此可知乙的方案更合理,
(3)加入略过量的铁屑,是将硫酸铜全部置换出来;
(4)如果铁过量,会混在红色粉末中,可以加入适量的酸除去剩余的铁屑.
故答案为:(1)CuO+H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+H2O,Fe+CuSO4═FeSO4+Cu;
(2)乙,甲方案第一步灼烧会产生污染空气的气体,粉尘,烟雾;
(3)确保CuSO4用完;
(4)将所得的铜粉酸洗后再洗涤,干燥.
点评 本题考查通过实验现象,综合利用所学知识进行分析解题的能力.


科目:初中化学 来源: 题型:选择题
| A. | Fe2O3 | B. | Fe | C. | CO | D. | CO2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 甲烷在空气中燃烧生成水和二氧化碳 | |
| B. | 镁带在空气中燃烧生成黑色固体 | |
| C. | 硫在空气中燃烧,发出淡蓝色火焰 | |
| D. | 米汤中滴加碘盐溶液,会变蓝 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
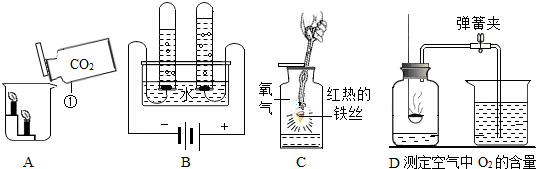
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氧气、五氧化二磷、乙醇汽油 | B. | 氮气、氯酸钾、白酒 | ||
| C. | 水银、二氧化硫、冰水混合体 | D. | 红磷、高锰酸钾、食醋 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 实验结论 | |
| 乙同学 实验 | 取中和反应后的溶液少许于试管中,将表面反复打磨后的铝片放入试管的溶液中 | 铝片逐渐溶解,并有大量气泡冒出,收集气体点燃,火焰呈淡蓝色 | 猜想Ⅱ成立 |
| 丙同学 实验 | 取中和反应后的溶液少许于试管中,向试管中滴加几滴无色酚酞试液 | 溶液变红色 | 猜想Ⅲ成立 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com