
【题目】某化学兴趣小组的同学在学完酸和碱的化学性质实验后,做了如下实验,并对实验过程进行了探究:
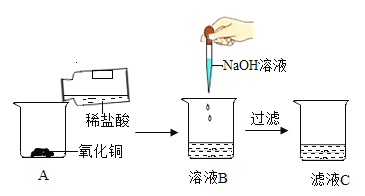
实验1:将一定量的稀盐酸倒人盛有氧化铜粉末的烧杯A中,实验观察到的现象是_______________,充分反应后得到溶液B。烧杯A中发生反应的化学方程式为___________________。
实验2:向溶液B中滴加一定量的氢氧化钠溶液,开始无明显现象,一段时间后发现溶液中出现了蓝色沉淀,过滤后得到滤液C。
[提出问题]滤液C中含有哪些溶质?
[猜想与假设]
小可认为:含有NaCl;
小凡认为:含有NaCl和HCl;
小燕认为:含有NaCl和NaOH;
小楠认为:含有_______________。
[讨论与交流](1)同学们经过讨论后,--致认为小凡的猜想不正确,你认为其中的理由是______________。
(2)小可经过观察,发现滤液C呈无色,认为自己的猜想正确,小楠的猜想是错误的。经过讨论,同学们也否定了小可的观点,原因是_______________。
(3)当向溶液B中滴加氢氧化钠溶液的过程中,刚开始出现蓝色沉淀时,溶液B中所含的离子是__________。
实验3:小楠取滤液C于试管中,加入无色酚酞溶液,观察到的现象为______________。于是同学们得出了结论:小燕的猜想正确。
[反思拓展](1)探究反应后所得溶液的溶质成分时,不仅要考虑生成物,还要考虑反应物是否过量。
(2)上述实验体现酸的两个化学性质,即酸能与金属氧化物反应、酸能与碱反应。
【答案】黑色粉末逐渐溶解,溶液由无色变为蓝色 ![]() NaCl和CuCl2 如果滤液中含有HCl,则不可能产生蓝色沉淀 氯化铜溶液蓝色,小楠的猜想错误,氯化钠、氢氧化钠均为无色,也可能是小燕的猜想正确。 Na+ 、Cu2+、Cl- 溶液变红
NaCl和CuCl2 如果滤液中含有HCl,则不可能产生蓝色沉淀 氯化铜溶液蓝色,小楠的猜想错误,氯化钠、氢氧化钠均为无色,也可能是小燕的猜想正确。 Na+ 、Cu2+、Cl- 溶液变红
【解析】
(1)氧化铜与稀盐酸反应生成氯化铜和水,观察到的现象为黑色粉末逐渐溶解,溶液由无色变为蓝色,反应的化学方程式为![]() 。
。
(2)根据实验1可知:稀盐酸与氧化铜反应生成氯化铜和水,若氯化铜过量,滤液C还可能是NaCl和CuCl2。
(3)如果滤液中含有HCl,则不可能产生蓝色沉淀,所以小凡的猜想不正确;
(4)因为滤液C是无色的,说明没有氯化铜,小楠的猜想错误;但氢氧化钠也为无色,无法确定溶液中是否含有氢氧化钠,所以小燕的猜想可能正确
(5)向溶液B中滴加一定量的氢氧化钠溶液,开始无明显现象,说明A烧杯中溶液的溶质为氯化铜、氯化氢。当溶液B中刚开始出现蓝色沉淀,说明氢氧化钠将过量的盐酸反应完,生成氯化钠,NaOH开始与氯化铜反应。所以溶液中所含的离子为Na+ 、Cu2+、Cl-。
(6)根据滤液C中加入酚酞溶液,得出小燕的猜想正确,即溶液中除氯化钠外,还有氢氧化钠,则加入酚酞溶液后,溶液变成红色。


 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:初中化学 来源: 题型:
【题目】如图是实验室制取气体的部分装置。
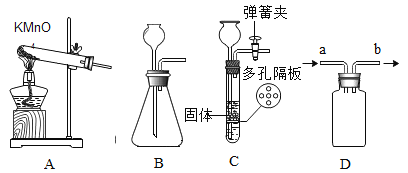
(1)写出实验室用A装置制取O2的化学反应方程式_______。
(2)B和C装置均可制取CO2,C装置与B装置相比其优点是什么_______?
(3)若用D装置采用排空气法收集O2,气体从a端进人,请把D装置图补画完整_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小明将未经砂纸打磨的铝条放入盛有稀盐酸的密闭容器中,用压强传感器测得容器内压强和反应时间的变化曲线如图所示,下列分析正确的是

A. AB 段表示铝与盐酸反应
B. CD 段压强变化的主要影响因素是温度
C. C 点生成的氢气质量大于 D 点
D. D 点处反应刚好结束
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验是进行科学探究的重要方式,根据下列图示回答相关问题:
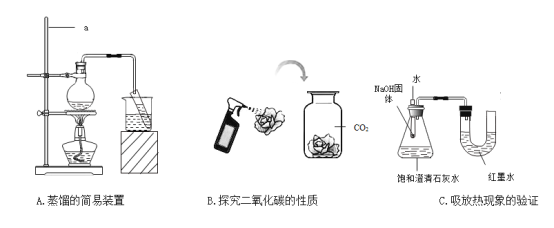
(1)实验A:仪器a的名称是___________;该简易装置的原理是利用物质的____________不同将各成分分离,得到的水是___________(填“纯净物”或“混合物”);
(2)实验B:将由石蕊试液染成紫色的干燥纸花喷水后放入装有二氧化碳的集气瓶中,观察到纸花变红,其原因用化学方程式表示为_____________。
(3)实验C:当向小试管中加入水后,观察到的现象为________,说明氢氧化钠在溶解过程中____________,(填“吸收”或“放出”)热量。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阅读下面短文,回答问题。
页岩气
随着社会对清洁能源需求不断扩大,天然气价格不断上涨,人们对页岩气的认识迅速提高。特别是水平井与压裂技术水平不断进步,人类对页岩气的勘探开发正在形成热潮。页岩气是指赋存于富有机质泥页岩及其夹层中,以吸附和游离状态为主要存在方式的非常规天然气,成分以甲烷为主,是一种清洁、高效的能源资源和化工原料,主要用于居民燃气、城市供热、发电、汽车燃料和化工生产等,用途广泛。我国页岩气资源潜力大,初步估计我国页岩气可采资源量在36.1万亿立方米,与常规天然气相当。
(1)页岩气属于________(填“可再生”或“不可再生”)能源。
(2)页岩气燃烧是将化学能转化为___________。
(3)若页岩气的热值为![]() ,则燃烧5L页岩气放出的热量为___________J。
,则燃烧5L页岩气放出的热量为___________J。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】芯片是所有电脑、智能家电的核心部件,它是以高纯度的单质硅(元素符号为Si)为材料制成的。用化学方法制得高纯硅的反应原理为:①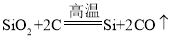 ②
②![]() ③
③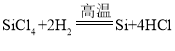 。请回答:
。请回答:
(1)在上述反应中属于置换反应的是_____(填序号)。
(2)标出SiCl4中硅元素的化合价_____。
(3)反应①中碳单质表现了_____性(填“氧化”或“还原”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在小明老家至今还有用作贮藏的地窖,当他学过二氧化碳知识后,及时科普了爷爷、奶奶,并且还主动参与了当地的课外活动小组,他们共同完成了如下实验探究。请回答下列问题:
(1)人若要进入久未开启的地窖,首先要做的实验是___
A用手电筒照明 B手持燃着蜡烛
C端入一大盆水 D把狗狗推进去
(2)同学们对地窖充满了好奇,决定要设计方案亲自测出其中二氧化碳的体积分数。
①取样:从地窖中用集气瓶迅速取回一瓶气体样品的方法是_________________________。
②测定:用150mL的注射器从集气瓶中抽取100mL气体样品,用下图所示装置进行实验。待推出所有气体并充分反应后,量筒内水的体积为99mL。
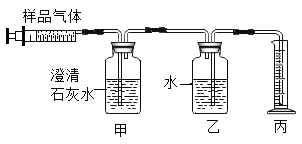
③估算:地窖中二氧化碳的体积分数为__________,若较长时间在里面停留,对人体产生的不适症状为_______________。
(3)若要进入含CO2较多的地方,应采取的措施是____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2018年10月24日上午9时,“新世界七大奇迹之一”的港珠澳大桥正式通车运营。

(1)大桥的建造采用了巨型预制组件方式,吊装的吊线主要成分是超高相对分子质量的聚乙烯纤维,其强度是普通尼龙绳的20倍,聚乙烯纤维属于_______________(填“合成纤维”或“天然纤维”)。生活中鉴别尼龙与棉线的方法是_______________。
(2)大桥发泡剂保温材料使用了偶氮二甲酰胺(化学式为C2 H4N4O2)。偶氮二甲酰胺分子中碳、氢元素的原子个数比为_______________,偶氮二甲酰胺中氮元素的质量分数为___________(精确到0.1%);
(3)大桥主梁使用钢板42万吨,钢属于铁的合金,工业上用一氧化碳与赤铁矿(主要成分为氧化铁)反应冶炼铁,反应的化学方程式为________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图象能正确反映对应变化关系的是( )
A. 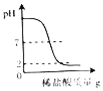 向一定量的氢氧化钠溶液中滴入pH=2的稀盐酸
向一定量的氢氧化钠溶液中滴入pH=2的稀盐酸
B. 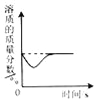 某温度时,向一定量的饱和石灰水中加入少量生石灰
某温度时,向一定量的饱和石灰水中加入少量生石灰
C.  向含有盐酸的氯化铜溶液中滴加烧碱溶液
向含有盐酸的氯化铜溶液中滴加烧碱溶液
D. 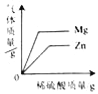 向等质量的镁、锌中,分别加入同浓度的稀硫酸
向等质量的镁、锌中,分别加入同浓度的稀硫酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com