
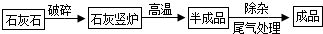
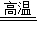 CaO+CO2↑
CaO+CO2↑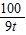 =
= ,
,

 科学实验活动册系列答案
科学实验活动册系列答案科目:初中化学 来源: 题型:
| A、正常雨水的pH为5.6的原因CO2+H2O═H2CO3 | B、用盐酸除去铁器表面的铁锈FeO+2HCl═FeCl2+H2O | C、工业上用煅烧石灰石的方法制生石灰CaCO3═CaO+CO2 | D、证明铁的金属活动性比氢强2Fe+3H2SO3═Fe2(SO4)3+3H2↑ |
查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
| ||
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com