
| 反应前 | 反应后 | |
| 烧杯及其中物质的质量 | 170.0g | 169.8g |
分析 (1)根据金属活动性顺序表及其应用分析,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来;
(2)根据铁会与硫酸反应生成硫酸亚铁和氢气,反应后烧杯中减少的质量就是氢气的质量,然后结合化学方程式计算出参加反应的硫酸的质量,再计算质量分数.
解答 解:(1)①由金属活动性顺序表及其应用可知,运用稀盐酸首先可验证镁比铁活泼,镁、铁比铜、银活泼.因为稀盐酸和铁镁能反应生成氢气,而铜银与稀盐酸不反应不产生氢气,且镁比铁产生氢气的速度快.但不能验证铜和银的金属活动性.利用金属活动顺序表中前面的金属能把后面的金属从它的化合物的溶液中置换出来,可用硝酸银溶液来比较铜银的活动性;
②说明Mg比Fe活泼的实验现象是:镁与稀盐酸反应速度比铁与稀盐酸反应速度快;
③说明Cu比Ag活泼的实验现象是:铜丝放入硝酸银溶液中,铜丝的表面有银白的金属生成;
(2)根据质量守恒定律可知,生成氢气的质量为:170g-169.8gg=0.2g;
设参加反应的硫酸的质量为x,
Fe+H2SO4=FeSO4+H2↑
98 2
x 0.2g
$\frac{98}{x}$=$\frac{2}{0.2g}$
x=9.8g
所以稀硫酸中溶质的质量分数是:$\frac{9.8g}{98g}$×100%=10%.
故答案为:(1)①硝酸银溶液;
②与酸反应镁比铁剧烈;
③铜丝表面有一层银白色物质生成;
(2)0.2g,10%.
点评 该题难度适中,主要考查了对金属活动性顺序的灵活运用,及根据化学方程式进行有关的计算,培养学生应用知识的能力.


科目:初中化学 来源: 题型:解答题
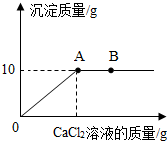 现有NaCl和Na2CO3混合物22.3克,加水完全溶解,形成99克溶液,往该溶液中逐滴加入10%的CaCl2溶液,产生沉淀的质量和所加CaCl2溶液的质量关系如图所示,求
现有NaCl和Na2CO3混合物22.3克,加水完全溶解,形成99克溶液,往该溶液中逐滴加入10%的CaCl2溶液,产生沉淀的质量和所加CaCl2溶液的质量关系如图所示,求查看答案和解析>>
科目:初中化学 来源: 题型:解答题
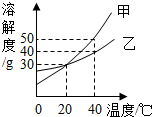 如图为甲、乙两种物质的溶解度曲线,请回答下列问题:
如图为甲、乙两种物质的溶解度曲线,请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 碱的溶液呈碱性,则碱性液体一定是碱的溶液 | |
| B. | 中和反应生成盐和水,则生成盐和水的反应一定是中和反应 | |
| C. | 单质中只含有一种元素,则只含有一种元素的纯净物一定是单质 | |
| D. | 碳酸盐与盐酸反应生成气体,则与盐酸反应生成气体的物质一定是碳酸盐 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 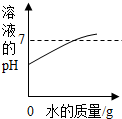 向一定量稀硫酸中滴加水 | |
| B. |  向一定量纯碱和烧碱的混合溶液中滴入盐酸 | |
| C. | 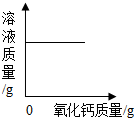 一定温度时向一定量饱和石灰水中加入氧化钙 | |
| D. | 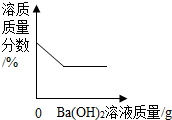 向稀硫酸中慢慢滴加Ba(OH)2溶液至过量 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①②⑤ | B. | ②③⑤ | C. | ③⑤⑦ | D. | ⑤⑦⑧ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com