
| A��Ũ��������100g 9.8%��ϡ���� | B���������������ʵ�ȥ�� |
| ��1��ʵ����Ҫ5.4mLŨ�����90mLˮ����ȡ����Һ���õ��������Тݢޢࣨ����ţ��� ��2��ϡ��ʱ���轫Ũ���Ỻ������ˮ�У������Ͻ��н��裬��ԭ����Ũ�����ܶȱ�ˮ������ˮ�ų������ȣ��ò��������Ͻ��裬ɢ�ȣ���ֹҺ�ηɽ��� | ��1��������Ҫ�õ��������Тڢ�⑪⑫������ţ��� ��2�����������У��費�Ͻ��н��裬��ԭ���Ƿ�ֹ�ֲ��¶ȹ��ߣ����Һ��ɽ��� |
| �ɹ�ѡ�����Ҫ������ ���Թ� ���ձ� �������� ��������ƽ ��10mL��Ͳ ��100mL��Ͳ ��ҩ�� �ེͷ�ι� ��©�� ��ƾ���⑪����̨⑫������ | |
���� A��1��������ͲҺ��һ��ʹ����Ͳ�����з������
��2������Ũ�����ϡ�ͷ���������ˮ�������ڣ������������Ͻ��������з������
B��1�����ǰѲ�����Һ��Ĺ�����Һ������һ�ַ��������ݹ��˲���������������з������
��2����������������ע��������з������
��� �⣺A��1��ʵ����Ҫ5.4mLŨ�����90mLˮ����Ͳ����ѡ������������㣺һ�DZ�֤��ȡһ�Σ�����������Һ���ȡ������ӽ�����ȡ����Һ���õ���������10mL����Ͳ��100mL����Ͳ�������㵹����Һ�����̶��ߣ��ٸ��ý�ͷ�ιܼ�Һ���̶��ߣ�
��2��ϡ��Ũ����ʱ��Ҫ��Ũ���Ỻ����������ע��ˮ�У�ͬʱ�ò��������Ͻ��裬��ʹ������ʱ����ɢ���в��ɰ�ˮע��Ũ�����У�������ΪŨ������ܶȱ�ˮ���������˳��ߵ�����ôˮ�ḡ��ˮ���ϣ�������Ũ��������ˮ�ų��������ȣ���ʹˮ���ڣ����������Һ�ɽ���
B��1�������ǰѲ�����Һ��Ĺ�����Һ������һ�ַ��������˲�����װ��������̨���ձ�����������©������������ɣ�
��2������ʱ��Ӧ�ò��������Ͻ��裬�Է�ֹ�ֲ��¶ȹ��ߣ����Һ��ɽ���
�ʴ�Ϊ��A��1���ݢޢࣻ��2��Ũ�����ܶȱ�ˮ������ˮ�ų������ȣ��ò��������Ͻ��裬ɢ�ȣ���ֹҺ�ηɽ���
B��1���ڢ�⑪⑫����2����ֹ�ֲ��¶ȹ��ߣ����Һ��ɽ���
���� �����ѶȲ�����������������ע�����Ũ�����ϡ�ͷ�������Ͳ��ʹ�÷����Ȳ��������������ȷ�����Ĺؼ���


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CO�ǻ�ԭ�� | B�� | C������ԭ��Ӧ | ||
| C�� | SnO2�������� | D�� | SnO2����������Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
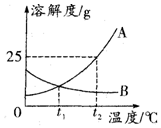 ��ͼΪA��B���ֹ������ʵ��ܽ�����ߣ�
��ͼΪA��B���ֹ������ʵ��ܽ�����ߣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
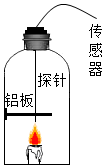 ������Ҫ��C��H��OԪ�أ����ܱ�������Ϩ���ԭ����ʲô��ȼ�յIJ�����ʲô��С����Ϊ����Ϩ���ԭ����ȼ���������������ڵ�����������ȼ�ղ���������룺
������Ҫ��C��H��OԪ�أ����ܱ�������Ϩ���ԭ����ʲô��ȼ�յIJ�����ʲô��С����Ϊ����Ϩ���ԭ����ȼ���������������ڵ�����������ȼ�ղ���������룺| ���ʪ�� | �������� | ������̼���� | һ����̼���� | |
| �����ȼǰ | 48.4% | 18.7% | 0.058% | 0 |
| ����Ϩ��� | 71.6% | 15.6% | 3.643% | 0.0182% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��------------ˮ�� | B�� | ������-------��ʯ�� | ||
| C�� | ̼������-----С�մ� | D�� | ��������-----��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ˮ����� | B�� | �ƾ���Һ | C�� | ������Ȫˮ | D�� | �����Ŀ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��˵������Ⱥ�֡�������ۡ�����ѧҩƷ��Ҳһ����ͬ����ҩƷ����ͬһ��������
��˵������Ⱥ�֡�������ۡ�����ѧҩƷ��Ҳһ����ͬ����ҩƷ����ͬһ��������| ҩƷ�� | һ�Ź� | Cu Mg Fe |
| ���Ź� | C P S | |
| ���Ź� | CO2 MgO CuO | |
| �� | H2SO4 HNO3 HCl | |
| ��Ź� | NaOH Ca��OH��2 Na2CO3 | |
| ���Ź� | KMnO4 NaCl CuSO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���ձ� | ������ʯ | ��ϡ���� | ����Ӧ���ձ������� | |
| �������ˣ� | ��90 | ��8.5 | ��50 | 145.2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ���·�չ���ϼ������ƶ�������������
���·�չ���ϼ������ƶ��������������鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com